Transkript
21. Schweizerische Tagung für Phytotherapie, Baden, 23. November 2006
Differenzierte Wirkungen von Mistelextrakten auf Krebszellen
Angelika Viviani und Lukas Rist
Einleitung
In der anthroposophischen Medizin werden Mistelpräparate zur Behandlung von Krebs seit der Empfehlung durch Rudolf Steiner zu Anfang des letzten Jahrhunderts angewendet. Man schätzt, dass ein erheblicher Anteil der Krebspatienten in Ergänzung zu herkömmlichen Behandlungen (Chemotherapie, Bestrahlung, Chirurgie) sich für irgendeine Form von komplementärmedizinischer Anwendung entscheiden (Molassiotis et al., 2006a; Molassiotis et al., 2006b; Molassiotis et al., 2006c; Molassiotis et al., 2006d). Von den verschiedenen komplementärmedizinischen Behandlungen gegen Krebs wird die Misteltherapie am häufigsten eingesetzt. Auch wissenschaftlich stösst die Mistel auf grosses Interesse. Sie ist mit über 1500 Publikationen eine der am intensivsten untersuchten Pflanzen (Kienle et al., 2003; Kienle et al., 2006). Die bisher vorliegenden klinischen Studien werden aber kontrovers diskutiert und sind leider zum Teil qualitativ unbefriedigend. Aufgrund einer umfassenden systematischen Übersicht kommen Kienle, Kiene & Albonico (Kienle et al., 2006) zum Schluss, dass die parenterale Applikation von Mistelpräparaten insbesondere die Lebensqualität erhöhen und auch die Lebensdauer von Krebspatienten verlängern kann.
Seit der Einführung der Mistelextrakte in der Krebstherapie sind diese pflanzlichen Vielstoffgemische zu verschiedensten Formulierungen verarbeitet worden. Die Präparate unterscheiden sich dabei in der Wirtsbaumauswahl, den verwendeten Pflanzenteilen und der pharmazeutischen Verarbeitung. Jahreszeitlich bedingte Schwankungen der wichtigen Inhaltsstoffe Lektin und Viscotoxin werden bei den Herstellern anthroposophischer Mistelpräparate durch die Mischung von Sommer- und Winterernte ausgeglichen.
Damit bestehen für die Praxis besondere Herausforderungen, weil es eine grosse Anzahl unterschiedlicher Präparate gibt, von denen nicht bekannt ist,
Zellwachstum (% Kontroll-Proben)
DAOY UW-228
Zellwachstum (% Kontroll-Proben)
D341
Iscucin Abietis Iscucin Mali Iscucin Pini Iscucin Crataegi Iscucin Populi Iscucin Tiliae Iscucin Quercus Iscucin Salicis
D425
Zellwachstum (% Kontroll-Proben)
Zellwachstum (% Kontroll-Proben)
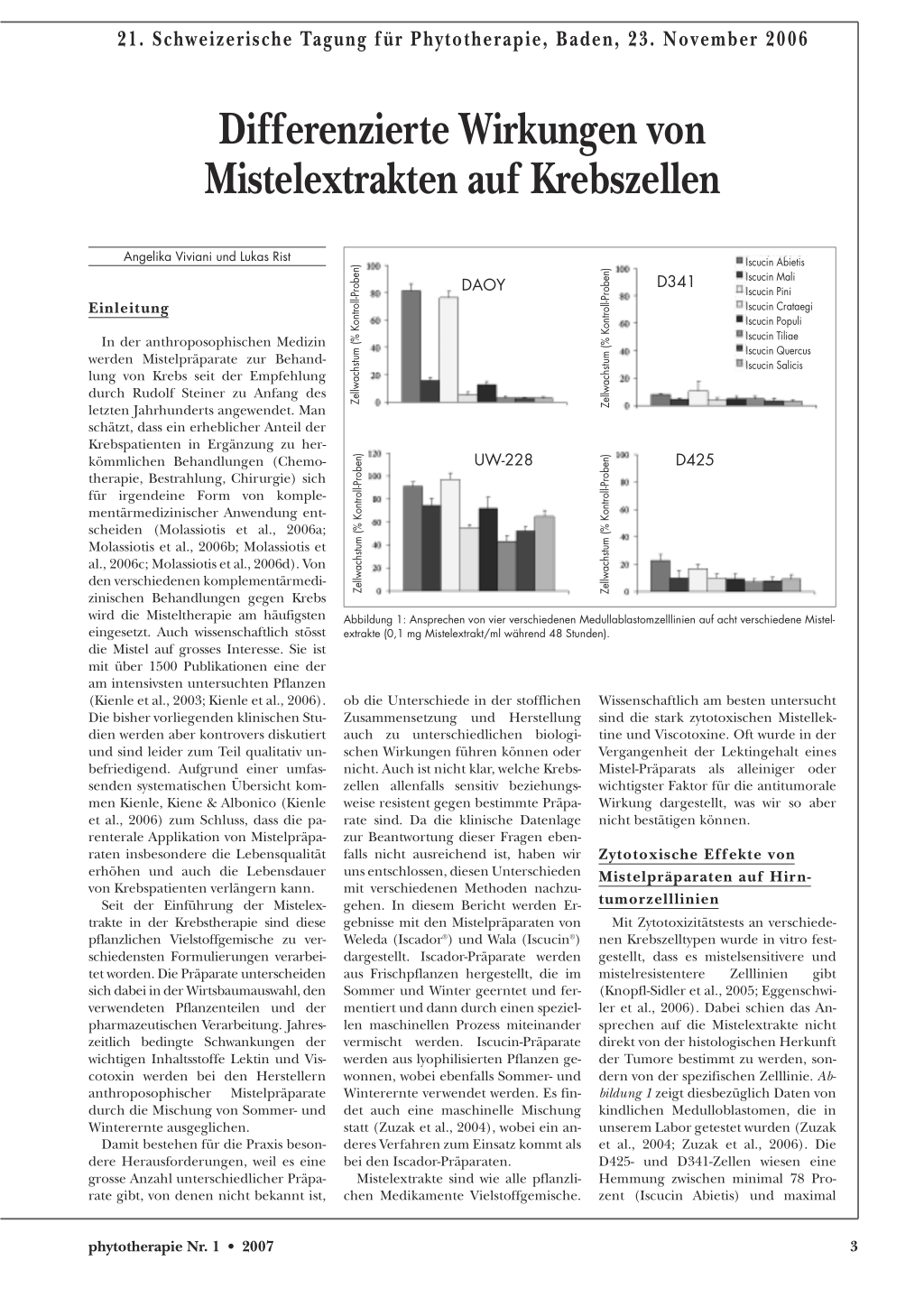
Abbildung 1: Ansprechen von vier verschiedenen Medullablastomzelllinien auf acht verschiedene Mistelextrakte (0,1 mg Mistelextrakt/ml während 48 Stunden).
ob die Unterschiede in der stofflichen Zusammensetzung und Herstellung auch zu unterschiedlichen biologischen Wirkungen führen können oder nicht. Auch ist nicht klar, welche Krebszellen allenfalls sensitiv beziehungsweise resistent gegen bestimmte Präparate sind. Da die klinische Datenlage zur Beantwortung dieser Fragen ebenfalls nicht ausreichend ist, haben wir uns entschlossen, diesen Unterschieden mit verschiedenen Methoden nachzugehen. In diesem Bericht werden Ergebnisse mit den Mistelpräparaten von Weleda (Iscador®) und Wala (Iscucin®) dargestellt. Iscador-Präparate werden aus Frischpflanzen hergestellt, die im Sommer und Winter geerntet und fermentiert und dann durch einen speziellen maschinellen Prozess miteinander vermischt werden. Iscucin-Präparate werden aus lyophilisierten Pflanzen gewonnen, wobei ebenfalls Sommer- und Winterernte verwendet werden. Es findet auch eine maschinelle Mischung statt (Zuzak et al., 2004), wobei ein anderes Verfahren zum Einsatz kommt als bei den Iscador-Präparaten.
Mistelextrakte sind wie alle pflanzlichen Medikamente Vielstoffgemische.
Wissenschaftlich am besten untersucht sind die stark zytotoxischen Mistellektine und Viscotoxine. Oft wurde in der Vergangenheit der Lektingehalt eines Mistel-Präparats als alleiniger oder wichtigster Faktor für die antitumorale Wirkung dargestellt, was wir so aber nicht bestätigen können.
Zytotoxische Effekte von
Mistelpräparaten auf Hirn-
tumorzelllinien
Mit Zytotoxizitätstests an verschiedenen Krebszelltypen wurde in vitro festgestellt, dass es mistelsensitivere und mistelresistentere Zelllinien gibt (Knopfl-Sidler et al., 2005; Eggenschwiler et al., 2006). Dabei schien das Ansprechen auf die Mistelextrakte nicht direkt von der histologischen Herkunft der Tumore bestimmt zu werden, sondern von der spezifischen Zelllinie. Abbildung 1 zeigt diesbezüglich Daten von kindlichen Medulloblastomen, die in unserem Labor getestet wurden (Zuzak et al., 2004; Zuzak et al., 2006). Die D425- und D341-Zellen wiesen eine Hemmung zwischen minimal 78 Prozent (Iscucin Abietis) und maximal
phytotherapie Nr. 1 • 2007
3
21. Schweizerische Tagung für Phytotherapie, Baden, 23. November 2006
97 Prozent (Iscucin Populi) auf. Die UW-228-Zellen reagierten verhältnismässig schwach mit Hemmungen zwischen 2 Prozent (Iscucin Pini) und 55 Prozent (Iscucin Tiliae). Die Wirkung der verschiedenen Präparate auf die DAOY-Zellen variierte stark. Die Zellproliferation wurde durch die Nadelbaumpräparate Iscucin Abietis und Pini nur um 18 Prozent respektive 22 Prozent erniedrigt, bei den Laubbaum-Präparaten jedoch um bis zu 97 Prozent.
Wie erwähnt ist bekannt, dass zahlreiche Inhaltsstoffe der Mistel in Abhängigkeit vom jeweiligen Wirtsbaum quantitativ stark schwanken können. Dies betrifft auch die Mistellektine I, II und III, die zytotoxisch und Apoptoseinduzierend wirken. Die auf den Nadelbäumen Kiefer und Tanne beheimateten Viscum-album-Unterarten gelten als lektinarm, bei den Laubholzmisteln ist hingegen mit höheren Gehalten und einer grösseren Bandbreite zu rechnen.
Die Lektingehalte verschiedener Iscucin-Präparate wurden mittels AC-2ELISA ermittelt. Tabelle 1 zeigt die Gesamtlektingehalte von 8 IscucinPräparaten. Vergleicht man die Ergebnisse aus Abbildung 1 mit den Lektinwerten der entsprechenden IscucinPräparate, so wird klar, dass weitere Mistel-Inhaltsstoffe, wie zum Beispiel die Viscotoxine und andere, die Wirkung mitbeeinflussen. Die Lektinwerte allein erlauben keine Aussage darüber, welches Präparat bei welchem Zelltyp die beste Wirkung erzielt.
Zytotoxische Effekte von
Mistelpräparaten auf Brust-
tumorzelllinien
Die Konzentration eines Extraktes, die das Zellwachstum auf 50 Prozent zu reduzieren vermag, wird als IC50-Wert bezeichnet. Je tiefer diese Konzentration ist, desto stärker wirkt der Extrakt. In Tabelle 2 sind diese IC50-Werte nach 48 Stunden für verschiedene IscadorPräparate bei unterschiedlichen Brustkrebszellen dargestellt (Eggenschwiler et al., submitted for publication). Während das Zellwachstum nach Behandlung mit jeder der 4 IscadorPräparate verringert wurde, schwankte der Umfang dieser Verringerung deutlich, je nach getestetem Iscador-Präparat und in Abhängigkeit der jeweiligen Zelllinie. Das lektinarme Iscador P (ca. 1 ng Lektin/mg Extrakt) verursachte den schwächsten Effekt auf alle Zelllinien. Interessanterweise zeigte das
ebenfalls lektinarme Iscador A je nach Zelllinie einen vergleichbaren oder sogar stärkeren Effekt als die Präparate Iscador Qu und M, die um einen Faktor von ca. 20 bis 40 lektinreicher sind.
Zytotoxizität von Mistel-
präparaten auf primäre
Kulturen von Brusttumoren
Bei den bisher geschilderten Ergebnissen handelte es sich immer um Zelllinien, mit denen typischerweise im Labor gearbeitet wird, weil sie einfach zu beschaffen und relativ leicht zu kultivieren sind. Allerdings handelt es sich auch um Zelllinien, die schon vor langer Zeit isoliert und seither im Labor weitergezüchtet werden und daher nur beschränkt repräsentativ für originäre Tumorzellen sind. Aus dem Grund sollten mit Zelllinien gewonnene Daten durch Daten von Experimenten mit sogenannten Primärkulturen, die von frisch operierten Brustkrebspatientinnen stammen, wo möglich ergänzt werden. In Abbildung 2 sind die Daten aus solchen Primärkulturen dargestellt, die den zytotoxischen Effekt der untersuchten Iscador-Präparate betreffen (KnopflSidler et al., 2005). Damit konnte gezeigt werden, dass die verwendeten Iscador-Präparate in der Lage sind, auch primäre Brustkrebszellen in vitro in ihrem Wachstum zu hemmen. Weiter zeigte sich, dass Zellen, die von verschiedenen Patientinnen stammten, unterschiedliche Empfindlichkeiten gegenüber den getesteten Präparaten aufweisen (Abbildung 2).
Genexpressionsprofile von
Brustkrebszellen nach der
Behandlung mit Mistel-
präparaten
Wir haben festgestellt, dass anhand der Lektingehalte von Mistelpräparaten nicht abgeschätzt werden konnte, welche Präparate bei welchen Tumoren wirksam sind und welche nicht. Aus diesem Grund haben wir ergänzend dazu eine andere Strategie verfolgt, mit dem Ziel, diese Abschätzung später durchführen zu können. Dazu erstellten wir von verschiedenen Krebszellen, die Mistelextrakten ausgesetzt wurden, einen genetischen «Fingerabdruck» (mRNA-Expressionsprofil) mittels der cDNA-Microarray-Technik (Eggenschwiler et al., 2006). Bei vier Brustkrebszelllinien wurden so jeweils 41 000 Gene analysiert und jene ausgewählt, die
Tabelle 1:
Gesamtlektingehalte der IscucinPräparate (Stufe H). Diese Präparate beinhalten 50 mg Extrakt/ml
Iscucin
Iscucin Abietis Iscucin Mali Iscucin Pini Iscucin Crataegi Iscucin Populi Iscucin Tiliae Iscucin Quercus Iscucin Salicis
µg Lectin/ ml Extrakt 0,8 5,3 1,1 8,4 5,3 13,7 9,9 5,9
Zellwachstum (% Kontroll-Proben)
Zellwachstum (% Kontroll-Proben)
Iscadorpräparat (mg/ml)
Iscadorpräparat (mg/ml)
Iscadorpräparat (mg/ml) Abbildung 2: Ansprechen von Tumorzellen von drei verschiedenen Brustkrebspatientinnen auf zwei Mistelpräparate.
Zellwachstum (% Kontroll-Proben)
4 phytotherapie Nr. 1 • 2007
21. Schweizerische Tagung für Phytotherapie, Baden, 23. November 2006
Tabelle 2:
IWC5a0c-Whseturmte
verschiedener Iscador-Präparate betreffend das In-vitrovon Brustkrebszelllinien. Konzentrationsangaben in mg/ml.
Iscador Qu Iscador M Iscador P Iscador A
MFM-223 0,05 ± 0,017 0,12 ± 0,034 1,42 ± 0,247 0,07 ± 0,028
KPL-1 0,10 ± 0,013 0,12 ± 0,022 1,94 ± 0,278 0,31 ± 0,059
MCF-7 0,09 ± 0,024 0,12 ± 0,020 1,61 ± 0,248 0,10 ± 0,022
HCC-1937 0,11 ± 0,017 0,10 ± 0,020 2,14 ± 0,989 0,31 ± 0,019
Tabelle 3:
Umprogrammierung von Stoffwechselwegen
Pathway (Anzahl Gene) Apoptose (95)
Cytokine-cytokine receptor interaction (204) Wnt signalling (143)
MAPK signalling (239)
Focal adhesion (157)
Regulation of actin cytoskeleton (204)
Zellen
Qu M
A
HCC-1937 –
++ –
KPL-1
++ –
–
MCF-7
–
–
–
Mfm-223 –
++ ++
HCC-1937 +
+++ +
KPL-1
++ ++ –
MCF-7
–
++ ++
Mfm-223 –
++ –
HCC-1937 –
+++ –
KPL-1
++ +
++
MCF-7
–
+
++
Mfm-223 – – ++
HCC-1937 +++ +++ ++
KPL-1
++ –
–
MCF-7
++ +
+
Mfm-223 – + –
HCC-1937 – – –
KPL-1
+– –
MCF-7
+
–
++
Mfm-223 – + ++
HCC-1937 – – –
KPL-1
–––
MCF-7
–
–
++
Mfm-223 – + ++
P – – – – + – + + – + – – + – + + – – – + – – – –
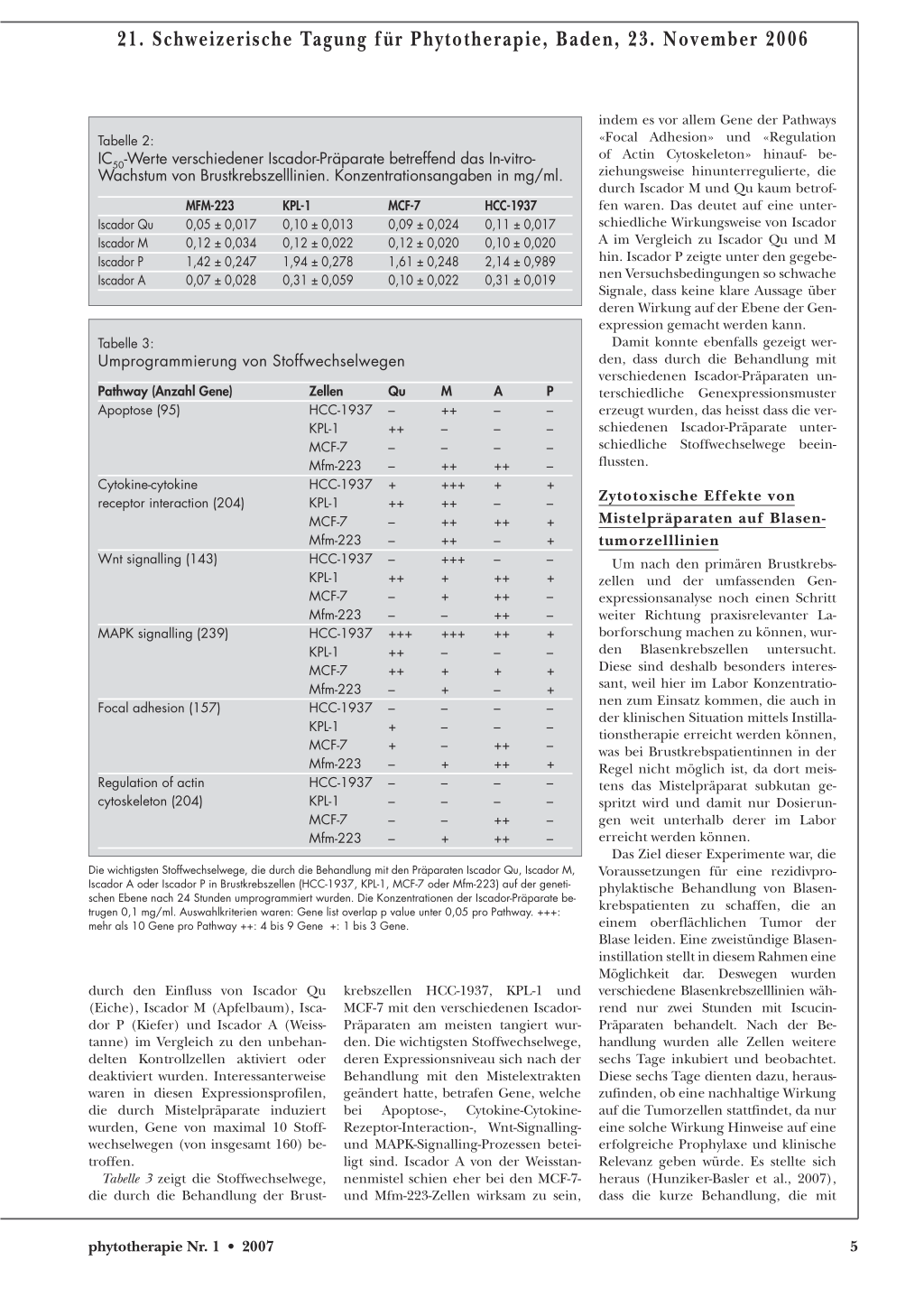
Die wichtigsten Stoffwechselwege, die durch die Behandlung mit den Präparaten Iscador Qu, Iscador M, Iscador A oder Iscador P in Brustkrebszellen (HCC-1937, KPL-1, MCF-7 oder Mfm-223) auf der genetischen Ebene nach 24 Stunden umprogrammiert wurden. Die Konzentrationen der Iscador-Präparate betrugen 0,1 mg/ml. Auswahlkriterien waren: Gene list overlap p value unter 0,05 pro Pathway. +++: mehr als 10 Gene pro Pathway ++: 4 bis 9 Gene +: 1 bis 3 Gene.
durch den Einfluss von Iscador Qu (Eiche), Iscador M (Apfelbaum), Iscador P (Kiefer) und Iscador A (Weisstanne) im Vergleich zu den unbehandelten Kontrollzellen aktiviert oder deaktiviert wurden. Interessanterweise waren in diesen Expressionsprofilen, die durch Mistelpräparate induziert wurden, Gene von maximal 10 Stoffwechselwegen (von insgesamt 160) betroffen.
Tabelle 3 zeigt die Stoffwechselwege, die durch die Behandlung der Brust-
krebszellen HCC-1937, KPL-1 und MCF-7 mit den verschiedenen IscadorPräparaten am meisten tangiert wurden. Die wichtigsten Stoffwechselwege, deren Expressionsniveau sich nach der Behandlung mit den Mistelextrakten geändert hatte, betrafen Gene, welche bei Apoptose-, Cytokine-CytokineRezeptor-Interaction-, Wnt-Signallingund MAPK-Signalling-Prozessen beteiligt sind. Iscador A von der Weisstannenmistel schien eher bei den MCF-7und Mfm-223-Zellen wirksam zu sein,
indem es vor allem Gene der Pathways «Focal Adhesion» und «Regulation of Actin Cytoskeleton» hinauf- beziehungsweise hinunterregulierte, die durch Iscador M und Qu kaum betroffen waren. Das deutet auf eine unterschiedliche Wirkungsweise von Iscador A im Vergleich zu Iscador Qu und M hin. Iscador P zeigte unter den gegebenen Versuchsbedingungen so schwache Signale, dass keine klare Aussage über deren Wirkung auf der Ebene der Genexpression gemacht werden kann.
Damit konnte ebenfalls gezeigt werden, dass durch die Behandlung mit verschiedenen Iscador-Präparaten unterschiedliche Genexpressionsmuster erzeugt wurden, das heisst dass die verschiedenen Iscador-Präparate unterschiedliche Stoffwechselwege beeinflussten.
Zytotoxische Effekte von
Mistelpräparaten auf Blasen-
tumorzelllinien
Um nach den primären Brustkrebszellen und der umfassenden Genexpressionsanalyse noch einen Schritt weiter Richtung praxisrelevanter Laborforschung machen zu können, wurden Blasenkrebszellen untersucht. Diese sind deshalb besonders interessant, weil hier im Labor Konzentrationen zum Einsatz kommen, die auch in der klinischen Situation mittels Instillationstherapie erreicht werden können, was bei Brustkrebspatientinnen in der Regel nicht möglich ist, da dort meistens das Mistelpräparat subkutan gespritzt wird und damit nur Dosierungen weit unterhalb derer im Labor erreicht werden können.
Das Ziel dieser Experimente war, die Voraussetzungen für eine rezidivprophylaktische Behandlung von Blasenkrebspatienten zu schaffen, die an einem oberflächlichen Tumor der Blase leiden. Eine zweistündige Blaseninstillation stellt in diesem Rahmen eine Möglichkeit dar. Deswegen wurden verschiedene Blasenkrebszelllinien während nur zwei Stunden mit IscucinPräparaten behandelt. Nach der Behandlung wurden alle Zellen weitere sechs Tage inkubiert und beobachtet. Diese sechs Tage dienten dazu, herauszufinden, ob eine nachhaltige Wirkung auf die Tumorzellen stattfindet, da nur eine solche Wirkung Hinweise auf eine erfolgreiche Prophylaxe und klinische Relevanz geben würde. Es stellte sich heraus (Hunziker-Basler et al., 2007), dass die kurze Behandlung, die mit
phytotherapie Nr. 1 • 2007
5
21. Schweizerische Tagung für Phytotherapie, Baden, 23. November 2006
höheren, aber durchaus klinisch erreichbaren Konzentrationen durchgeführt wurde, je nach Präparat und Zelllinie äusserst wirksam sein kann. Im Fall von Iscucin Crataegi (Abbildung 3C) und auch von Iscucin Tiliae (Abbildung 3E) konnte ein starker und bis auf sechs Tage anhaltender Effekt bei allen Zelllinien festgestellt werden. Wenn man diese zwei sehr wirksamen IscucinPräparate miteinander vergleicht, fällt der ausgeprägte Effekt von Iscucin Crataegi auf.
Ähnliche Beobachtungen wurden auch mit Iscador-Präparaten beschrieben (Urech et al., 2006a).
In-vitro-Experimente lassen sich nur bedingt auf die In-vivo-Situation übertragen. Natürlicherweise sind in der Physiologie der Patienten für das Überleben und die Vermehrung der Tumorzellen noch andere Faktoren als in den experimentellen Versuchen massgeblich mitverantwortlich. Trotzdem zeigen diese Daten, dass es sich lohnt, entsprechende klinische Studien durchzuführen.
Schlussfolgerung
Die Vielfalt an unterschiedlichen Mistelpräparaten scheint prinzipiell ge-
rechtfertigt zu sein, da wir nachweisen konnten, dass die Unterschiede zwischen den verschiedenen Präparaten auch zu unterschiedlichen Hemmungen des Tumorzellwachstums bei den untersuchten Krebszelllinien und primären Brustkrebszellen führten. Weiter konnten wir zeigen, dass durch die verschiedenen Mistelpräparate auch tatsächlich verschiedene Stoffwechselwege beeinflusst wurden, das heisst dass die Mistelpräparate offenbar sehr spezifisch auf die Krebszellen wirkten. Aufgrund des Lektingehalts konnte nicht vorausgesagt werden, welches Präparat welche Wirkung haben würde, und es war auch nicht möglich, aufgrund der chemischen Zusammensetzung zu entscheiden, welche Tumorzellen mistelsensitiver oder mistelresistenter sein würden. Durch die weitere Anwendung der cDNA-Microarray-Technik wurde es möglich, mistelsensitive von mistelresistenten Tumoren zu unterscheiden und zu bestimmen, welche Tumore auf welche Präparate ansprechen könnten. Die Microarraytechnologie ist eine Methode, mit der prädiagnostisch das Ansprechen eines Tumors auf ein bestimmtes Mistelpräparat erfasst werden kann, mit der aber auch die Wirkungen
von Pflanzenextrakten untereinander verglichen werden können.
Danksagung
Die in diesem Manuskript zusam-
mengefassten Ergebnisse verdanken
wir zahlreichen Mitarbeitern. Für die
experimentelle Arbeit möchten wir
J. Eggenschwiler, T. J. Zuzak, N. Hunzi-
ker-Basler, L. von Balthazar, B. Stritt,
D. Pruntsch, F. Knöpfl-Sidler erwäh-
nen. Für die wissenschaftlichen
Schreibarbeiten und die Beratung
danken wir A. P. Simões-Wüst, K. Urech
und A. Hensel. Ohne die tatkräftige
Unterstützung der Firmen Weleda AG
(in der Person von M. Ramos F.) und
Wala Heilmittel GmbH (in der Person
von U. Meyer) wäre diese Arbeit nicht
möglich gewesen.
■
Anschrift der Referenten Prof. Dr. Angelika Viviani (Korrespondenzadresse) Hochschule Wädenswil Grüental 8820 Wädenswil E-Mail: a.viviani@hsw.ch
Dr. Lukas Rist Paracelsus-Spital Bergstr.16 8805 Richterswil
A) Abietis
VM-CUB1 TCC-SUP T-24 J82 UM-UC-3
B) Populi
VM-CUB1 TCC-SUP T-24 J82 UM-UC-3
C) Crataegi
VM-CUB1 TCC-SUP T-24 J82 UM-UC-3
Zellwachstum (% Kontroll-Proben)
Zellwachstum (% Kontroll-Proben)
Zellwachstum (% Kontroll-Proben)
Zellwachstum (% Kontroll-Proben)
Zeit (Stunden)
Zeit (Stunden)
Zeit (Stunden)
D) Quercus
Zeit (Stunden)
Zellwachstum (% Kontroll-Proben)
VM-CUB1 TCC-SUP T-24 J82 UM-UC-3
E) Tiliae
Zeit (Stunden)
VM-CUB1 TCC-SUP T-24 J82 UM-UC-3
Abbildung 3: Nachhaltigkeit der Wirkung von Iscucinpräparaten auf das Wachstum von fünf verschiedenen Blasenkrebszelllinien. Die Wirksamkeit der Präparate Iscucin® Abietis, Iscucin® Populi, Iscucin® Crataegi, Iscucin® Quercus und Iscucin® Tiliae wurde anhand der Wachstumshemmung der VM-CUB1, TCC-SUP-, T-24-, J82- und UM-UC-3-Blasenkarzinomzelllinien mit MTT-Tests erfasst (n = 3, 16-fach Bestimmungen pro Experiment). Dabei wurden die Zellen während 2 Stunden mit 8 mg Iscucinpräparat/ml inkubiert. Nach dem Entfernen des Mistelpräparates wurden die Zellen in frischem Kulturmedium weitergezüchtet. Die MTT-Tests wurden nach 24, 48, 72 und 144 Stunden zur Bestimmung der mitochondrialen Aktivität durchgeführt. Bitte bei dem Vergleich zum Teil unterschiedliche Y-Achsen berücksichtigen.
6 phytotherapie Nr. 1 • 2007
21. Schweizerische Tagung für Phytotherapie, Baden, 23. November 2006
Literaturreferenzen:
Eggenschwiler J, Patrignani A, Wagner U, Rehrauer H, Schlapbach R, Rist L, Ramos MH & Viviani A (2006) Gene expression profiles of different breast cancer cells compared with their responsiveness to fermented mistletoe (Viscum album L.) extracts Iscador from oak (Quercus), pine (Pinus), white fir (Abies) and apple tree (Malus) in vitro. Arzneimittelforschung 56, 483–496.
Eggenschwiler J, Stritt B, Pruntsch D, Rist L, Simões-Wüst A & Viviani A Mistletoe lectin is not the only cytotoxic component in fermented preparations of Viscum album from white fir (Abies). Submitted for publication.
Hunziker-Basler N, Zuzak TJ, Eggenschwiler J, Rist L, Simões-Wüst AP & Viviani A (2007) Prolonged cytotoxic effect of aqueous extracts from dried Viscum album on bladder cancer cells. Die Pharmazie. Accepted for publication.
Kienle GS, Berrino F, Bussing A, Portalupi E, Rosenzweig S & Kiene H (2003) Mistletoe in cancer – a systematic review on controlled clinical trials. Eur J Med Res 8, 109–119.
Kienle GS, Kiene H & Albonico HU (2006) Anthroposophic medicine: health technology assessment report – short version. Forsch Komplementarmed 13 Suppl 2, 7–18.
Knopfl-Sidler F, Viviani A, Rist L & Hensel A (2005) Human cancer cells exhibit in vitro individual receptiveness towards different mistletoe extracts. Pharmazie 60, 448–454.
Molassiotis A, Browall M, Milovics L, Panteli V, Patiraki E & Fernandez-Ortega P (2006a) Complementary and alternative medicine use in patients with gynecological cancers in Europe. Int J Gynecol Cancer 16 Suppl 1, 219–224.
Molassiotis A, Ozden G, Platin N, Scott JA, Pud D, Fernandez-Ortega P, Milovics L, Panteli V, Gudmundsdottir G, Browall M, Madsen E, Patiraki E & Kearney N (2006b) Complementary and alternative medicine use in patients with head and neck cancers in Europe. Eur J Cancer Care (Engl) 15, 19–24.
Molassiotis A, Panteli V, Patiraki E, Ozden G, Platin N, Madsen E, Browall M, Fernandez-Ortega P, Pud D & Margulies A (2006c) Complementary and alternative medicine use in lung cancer pa-
tients in eight European countries. Complement Ther Clin Pract 12, 34–39.
Molassiotis A, Scott JA, Kearney N, Pud D, Magri M, Selvekerova S, Bruyns I, FernadezOrtega P, Panteli V, Margulies A, Gudmundsdottir G, Milovics L, Ozden G, Platin N & Patiraki E (2006d) Complementary and alternative medicine use in breast cancer patients in Europe. Support Care Cancer 14, 260–267.
Urech K, Buessing A, Thalmann G, Schaefermeyer H & Heusser P (2006) Antiproliferative effects of mistletoe (Viscum album L.) extract in urinary bladder carcinoma cell lines. Anticancer Res 26, 3049–3055.
Zuzak T, Rist L, Viviani A, Eggenschwiler J, Mol C, Riegert U & Meyer U (2004) Das Mistelpräparat. Iscucin-Herstellung, Analytik, Wirkung in vitro. Der Merkurstab 57, 467–473.
Zuzak TJ, Rist L, Eggenschwiler J, Grotzer MA & Viviani A (2006) Paediatric medulloblastoma cells are susceptible to Viscum album (mistletoe) preparations. Anticancer Res 26, 3485–3492.
phytotherapie Nr. 1 • 2007
7