Transkript
Fortbildung
Klinisch-pharmakologische Besonderheiten und Fallstricke in der Therapie mit Antidepressiva
Klaus Mörike
Im vorliegenden Beitrag sollen einige klinisch-pharmakologische Gesichts-
deutlich sedierender Wirkung sowohl in verschiedenen chemischen als auch in verschiedenen pharmakologischen Gruppen enthalten sind.
punkte besprochen werden, die bei der Verschreibung von Antidepressiva wichtig sind, in bestimmten Situationen Bedeutung erlangen beziehungsweise Fallstricke darstellen können. Phasen-
Chemische Struktur
Insgesamt sind Antidepressiva chemisch sehr heterogen. Nach der chemischen Struktur werden unterschieden: ■ trizyklische Antidepressiva ■ tetrazyklische Antidepressiva ■ chemisch neuartige Antidepressiva. Trizyklische Antidepressiva enthalten die charakteristische Anordnung von drei Ringen und leiten sich vom Imipramin (Abbildung 1) ab.
prophylaktika («mood stabilizers»)
werden nicht behandelt.
D ie Depression ist weltweit eine der häufigsten und schwerwiegendsten Erkrankungen mit hohem Rückfallrisiko und erhöhter Sterblichkeit.» Mit diesen Worten beginnen die Empfehlungen zur Therapie der Depression, die die Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ, www.akdae.de) in zweiter Auflage im Jahr 2006 herausgegeben hat. Der Pharmakotherapie kommt ein wesentlicher Stellenwert im Rahmen des Gesamtkonzepts der Behandlung der Depression zu, und Antidepressiva werden in grossem Umfang verordnet.
Einteilung der Antidepressiva
Antidepressiva können nach verschiedenen Gesichtspunkten eingeteilt werden: ■ chemische Struktur ■ pharmakologischer Wirkmechanismus ■ klinische Wirkung.
Abbildung 1: Strukturformel von Imipramin mit der für trizyklische Antidepressiva charakteristischen Anordnung von drei Ringen.
(Quelle: Wikipedia)
Strukturchemische Abwandlungen, auch geringfügige, an den Ringen oder an der Seitenkette führen oft zu erheblichen Änderungen der pharmakologischen beziehungsweise klinischen Wirkung. Ausser Imipramin gehören zu den bekanntesten trizyklischen Antidepressiva Amitriptylin, Nortriptylin, Desipramin, Doxepin. Tetrazyklische Antidepressiva sind Maprotilin (Abbildung 2), Mianserin und Mirtazapin.
14
Die Kategorien sind nicht kongruent, das heisst Mittel mit einer bestimmten pharmakologischen Hauptwirkung können nicht notwendigerweise den Substanzen einer bestimmten chemischen Klasse zugeordnet werden und umgekehrt. Vor allem die klinische Wirkung ist nicht eindeutig mit einer chemischen Klasse verknüpft, normalerweise auch nicht mit der pharmakologischen Hauptwirkung. Dies bedeutet, dass Antidepressiva mit
Abbildung 2: Strukturformel
von Maprotilin (Quelle: Wikipedia)
Von den tri- und tetrazyklischen Antidepressiva abgegrenzt werden die chemisch neuartigen Antidepressiva. Sie zeigen untereinander keine strukturchemische Ähnlichkeit.
Psychiatrie 1•2008
Fortbildung
Der erste Fallstrick: Die chemische
Gruppenzugehörigkeit eines
Antidepressivums lässt nicht auf die
klinische Wirkung schliessen.
Pharmakologischer Wirkmechanismus Auf welche Weise Antidepressiva ihre antidepressive Wirkung ausüben, ist nicht eindeutig geklärt. Dies liegt auch wesentlich daran, dass die Pathophysiologie der Depression noch immer weitgehend unklar ist. Die Monoaminhypothese besagt, dass ein funktioneller Mangel von Monoamin-Neurotransmittern, insbesondere von Serotonin beziehungsweise Noradrenalin, in bestimmten Hirnregionen eine Rolle spielt. Die pharmakologische Beschreibung der Antidepressiva umfasst den Mechanismus, der diesem Monoaminmangel entgegenwirkt. Dies kann geschehen über ■ eine Hemmung der neuronalen Wiederaufnahme der
Neurotransmitter aus dem synaptischen Spalt in die terminalen Nervenendigungen ■ eine Steigerung der Freisetzung der Neurotransmitter aus den terminalen Nervenendigungen ■ eine Hemmung des Abbaus der Neurotransmitter.
Über die Monoaminhypothese hinaus gibt es neuere Erkenntnisse. Interesse finden Hypothalamus-HypophysenNebennierenrinden-Achse, Neurodegeneration, Neurogenese und Neuroplastizität. Einer oder mehrere dieser Angriffspunkte spielen bei den gegenwärtig eingesetzten Antidepressiva wahrscheinlich eine Rolle. Dessen ungeachtet folgt die aktuelle Einteilung der Antidepressiva den oben dargestellten Mechanismen (Tabelle 1).
Die Kategorisierung nach der pharmakologischen Hauptwirkung ist die am weitesten verbreitete Art der Einteilung der Antidepressiva. Leider lässt die Zugehörigkeit zu einer bestimmten pharmakologischen Gruppe keinen eindeutigen Schluss auf das klinische Wirkprofil (s. unten) zu.
Der zweite Fallstrick: Die pharmakologische Gruppenzugehörigkeit
eines Antidepressivums lässt nicht ohne Weiteres auf die klinische Wirkung schliessen.
Klinische Eigenschaften Neben der antidepressiven Wirkung umfasst das Wirkprofil der einzelnen Antidepressiva vielfach weitere Eigenschaften. Diese können – je nach Therapieziel – erwünscht oder unerwünscht sein. Ganz wesentlich bei den Begleitwirkungen ist die Sedierung. Ob ein Antidepressivum diese Qualität aufweist oder nicht und ob diese Wirkung bei dem betreffenden Patienten angestrebt wird (z.B. wegen agitierter Depression bzw. wegen Schlafstörungen) oder unerwünscht ist (z.B. für eine aktive Teilnahme am Berufsleben oder am Strassenverkehr), spielt für die Auswahl des für einen bestimmten Patienten vorgesehenen Wirkstoffs eine wichtige Rolle. Bei Amitriptylin, Trimipramin und Doxepin ist die sedierende Wirkung ausgeprägt, ebenso bei Mirtazapin. Bei SSRI, Reboxetin und MAO-I fehlt eine sedierende Wirkung weitgehend.
Tabelle 1:
Einteilung der Antidepressiva nach der pharmakologischen Hauptwirkung
Wirkstoffklasse1 NSMRI (nichtselektive Monoamin-Rückaufnahme-Inhibitoren)
SSRI (selektive Serotonin-Rückaufnahme-Inhibitoren)
SSNRI (selektive Serotonin- und Noradrenalin-RückaufnahmeInhibitoren) SNRI (selektive Noradrenalin-Rückaufnahme-Inhibitoren) NaSSA (Noradrenalin- und Serotonin-selektive Antidepressiva) MAO-I (Monoaminoxidase-Inhibitoren)
Wirkstoffe (wichtigste Vertreter)
Die meisten trizyklischen Antidepressiva2 (Amitriptylin, Nortriptylin, Imipramin, Desipramin, Doxepin, Clomipramin) Fluoxetin, Fluvoxamin, Citalopram und Escitalopram, Sertralin, Paroxetin Venlafaxin (überwiegender Serotonin-Rückaufnahme-Inhibitor), Duloxetin Reboxetin Mirtazapin (auch ␣2-Adrenozeptor-Antagonist) Moclobemid (selektiver und reversibler MAO-A-Inhibitor), Tranylcypromin (irreversibler MAO-I)
1 Darüber hinaus gibt es Antidepressiva, die nicht in eine dieser Kategorien passen, z.B. Johanniskrautextrakt, Trimipramin, Antidepressiva mit anderen (neuen) Wirkprinzipien.
2 Trizyklische Antidepressiva wirken als nichtselektive Monoamin-Rückaufnahme-Inhibitoren (NSMRI), jedoch mit unterschiedlichen Schwerpunkten bei den Neurotransmittern. Clomipramin hemmt überwiegend die Serotonin-Rückaufnahme. Bei Trimipramin ist die Monoamin-Rückaufnahme-Inhibition so schwach, dass dieses trizyklische Antidepressivum nicht zu den NSMRI gerechnet werden kann.
15
Psychiatrie 1•2008
Fortbildung
16
Unerwünschte Wirkungen
alpha-adrenolytischer Wirkungen. Dies ist einer der
Unerwünschte Wirkungen spielen für die Lebensqualität Hauptgründe, weshalb heute die SSRI gegenüber den
eine wesentliche Rolle und können die Therapietreue trizyklischen Antidepressiva vielfach als First-line-Mittel
(Compliance) entscheidend beeinträchtigen. Der Auf- bevorzugt werden.
klärung kommt hohe Bedeutung zu und wird auch den Hyponatriämie kann unter praktisch allen Antidepres-
Hinweis einschliessen, dass manche unerwünschte Wir- siva auftreten. Bei normovolämischen Patienten ist
kungen am Therapiebeginn eher betont sind und im wei- offenbar ein Syndrom der inadäquaten Sekretion von
teren Verlauf durchaus wieder abnehmen können. Um- antidiuretischem Hormon (SIADH) ursächlich beteiligt.
gekehrt tritt die antidepressive Wirkung
typischerweise nicht sofort, sondern erst
nach Wochen oder Monaten ein. Die Gründe für diese Verzögerung sind unklar.
Ein Beginn der Therapie mit niedrigen Dosen
Einige unerwünschte Wirkungen sollen
ist insbesondere bei älteren und alten
nachfolgend kurz besprochen werden: Die sedierende Wirkung ist, wie oben ausgeführt, bisweilen unerwünscht. Sie steht oft am Therapiebeginn eher im Vordergrund
Patienten ratsam, weil bei diesen Patienten erfahrungsgemäss die Empfindlichkeit für zentralnervös dämpfende Effekte und
als im weiteren Therapieverlauf. Möglicher-
Nebenwirkungen grösser als bei jüngeren ist
weise besteht ein Zusammenhang mit der Histamin-H1-antagonistischen und/oder Serotonin-5-HT-antagonistischen Wirkung.
und auch für die therapeutische Wirkung geringere Dosen ausreichen.
Auch Appetit- und Gewichtszunahme wer-
den damit in Verbindung gebracht.
Eine anticholinerge Wirkung gehört zum Wirkprofil der Die Hyponatriämie kann asymptomatisch bleiben oder
trizyklischen Antidepressiva. Sie äussert sich in vorwie- zentralnervöse Symptome (Kopfschmerzen, Lethargie,
gend in Mundtrockenheit, Miktionsstörungen (besonders Schwindel und Ataxie, Verwirrtheit, Psychose, Krampf-
bei älteren Männern mit Prostatahypertrophie), Obstipa- anfälle, Koma) bieten. Da diese Symptome unspezifisch
tion (u.U. bis hin zum Subileus) oder Akkommodations- sind, ist es wichtig, an die Möglichkeit einer Hyponatri-
störungen. Ein spezielles Problem, vor allem bei älteren ämie als unerwünschte Wirkung zu denken.
und alten Patienten, stellen kognitive Störungen dar. Ein Eine Verlängerung des QT-Intervalls im Elektrokardio-
sogenanntes anticholinerges Delir kann in seltenen Fäl- gramm wird mit erhöhtem Risiko sogenannter Torsades-
len auftreten.
de-pointes-(TdP-)Arrhythmien assoziiert. TdP können
Vor allem wegen der sedierenden und anticholinergen Wir- zu lebensbedrohlichen Kammertachykardien führen.
kungen von Amitriptylin wird dieser Wirkstoff in der soge- Neben genetischen Ursachen (angeborene Long-QT-
nannten «Beers-Liste» zu den potenziell ungeeigneten Mit- Syndrome; LQTS) können auch verschiedene Arzneimit-
teln für alte Patienten gerechnet (5). Diese Etikettierung ist tel, auch manche Psychopharmaka, zu einer QT-Verlän-
nicht unwidersprochen, zeigt aber zumindest an, dass Ami- gerung und erhöhtem TdP-Risiko führen. Amitriptylin ist
triptylin für einige alte Patienten ein problematischer Wirk- mit QT-Verlängerung in Verbindung gebracht worden.
stoff sein kann. Hinzu kommt eine alpha-adrenolytische Ein erhöhtes TdP-Risiko wird bei therapeutisch korrek-
Wirkung, die sich in Hypotension beziehungsweise ortho- ter Anwendung als unwahrscheinlich eingestuft, jedoch
statischen Blutdruckregulationsstörungen manifestiert.
sollten Amitriptylin und verwandte Trizyklika sowie
Ein erhöhtes Sturzrisiko zeigte sich in einigen Studien einige SSRI bei Patienten mit angeborenem LQTS gemie-
für trizyklische Antidepressiva und auch für SSRI. Der den werden (Informationen zu Arzneimitteln und LQTS
Pathomechanismus ist unklar. Für ältere und alte Patien- finden sich auf der Website der University of Arizona
ten ist das erhöhte Risiko für Stürze beziehungsweise www.qtdrugs.org).
Schenkelhalsfrakturen ein ausserordentlich wichtiges Viel diskutiert wurde in den letzten Jahre über die Frage,
Sicherheitsproblem.
ob Antidepressiva eine Suizidalität auslösen beziehungs-
Sexualstörungen sind weitere potenzielle unerwünschte weise verstärken können. Insgesamt gesichert ist dies
Wirkungen von Antidepressiva. Bei den SSRI und Ven- nicht, aber es kann bei einzelnen Patienten zu Beginn
lafaxin sind sie eine der häufigsten unerwünschten Wir- der antidepressiven Behandlung ein zunehmendes oder
kungen. Im Einzelfall kann es schwierig sein, eine auch neu auftretendes Risiko suizidalen Verhaltens
Sexualstörung einer Arzneimittelwirkung beziehungs- bestehen. Ein entsprechendes Monitoring, vor allem zu
weise der Grunderkrankung zuzuordnen.
Beginn der Therapie, ist wichtig. Die Diskussion sollte
Vorteilhaft bei den SSRI ist das Fehlen anticholinerger nicht dazu führen, ein Antidepressivum bei vorliegender
(Ausnahme: Paroxetin wirkt schwach anticholinerg) und Indikation vorzuenthalten.
Psychiatrie 1•2008
Fortbildung
Tabelle 2:
Arzneimittel, die mit einem Serotoninsyndrom assoziiert wurden
SSRI: alle
Andere Antidepressiva: Trazodon, Buspiron, Clomipramin, Venlafaxin, Lithium
MAO-Hemmer:
Moclobemid u.a.
Antikonvulsiva:
Valproinsäure
Analgetika:
Fentanyl, Tramadol, Pentazocin, Meperidin
Antiemetika:
Ondansetron, Granisetron, Metoclopramid
Migränemittel:
Sumatriptan
Erkältungsmittel:
Dextromethorphan
Drogen:
«Ecstasy», LSD, «Foxy Methoxy»
Pflanzliche Mittel: Johanniskrautextrakt, Ginseng
Einige Kombinationen:
Linezolid (antibakterielles Mittel mit MAO-I-Wirkung) + Citalopram Tranylcypromin + Imipramin Moclobemid + SSRI Tramadol, Venlafaxin + Mirtazapin
nach: Boyer EW, Shannon M: The serotonin syndrome. N Engl J Med 352 (11), 1112–1120 (2005)
Selten können SSRI das Auftreten von Blutungen (z.B. gastrointestinal) begünstigen. Dies wird auf die Hemmung der Serotoninaufnahme in die Thrombozyten zurückgeführt. Das Risiko ist beim gleichzeitigen Gebrauch von Acetylsalicylsäure (auch niedrig dosiert) oder nichtsteroidalen Antirheumatika höher. Das sogenannte Serotoninsyndrom ist eine seltene, aber ernste Komplikation (Tabelle 2). Es resultiert aus der Überstimulation von Serotoninrezeptoren und ist klinisch charakterisiert durch Übelkeit, Diarrhö, Unruhe/ Agitiertheit, Hyperreflexie, autonome Instabilität, Myoklonus, Muskelrigidität, Hyperthermie, Delir, Krampfanfälle. In schweren Fällen kommt es zu Herz-Kreislaufbeziehungsweise Multiorgan-Versagen und Tod. Das Serotoninsyndrom kommt am ehesten beim Zusammenwirken bestimmter Arzneimittel (z.B. MAO-I mit serotonergen Mitteln wie SSRI) vor, es sind aber auch Fälle nach einer einzelnen therapeutischen Dosis eines SSRI berichtet worden (7).
Plasmakonzentrationsbestimmung
Für die Wirkungen vieler Arzneimittel ist die Konzentration wesentlich, und die Konzentration am Wirkort (z.B. Gehirn) steht mit der Konzentration im Plasma in proportionalem Verhältnis. Für viele, wenngleich nicht alle
Fortbildung
18
Die Dosis-Wirkungs-Beziehung und die Bedeutung der Plasmakonzentration
Pharmakokinetik
Pharmakodynamik
Dosis Konzentration Wirkung
Clearance, Verteilungsvolumen,
Bioverfügbarkeit
z.B. Ausprägung von Zielstrukturen der Arzneimittelwirkung
Abbildung 3: Die Dosis-Wirkungs-Beziehung und ihre Einflussfaktoren. Die Clearance eines
Patienten, eine wichtige individuelle Eigenschaft, bestimmt wesentlich die Dosis-Konzentrations-
und damit die Dosis-Wirkungs-Beziehung. Bei Arzneimitteln, für welche die Konzentrations-
Wirkungs-Beziehung gut etabliert ist, kann bei Kenntnis der Konzentration die individuelle Dosis-Wirkungs-Beziehung charakterisiert und
durch Dosisanpassung optimiert werden.
Antidepressiva sind Konzentrations-Wirkungs-Beziehungen gezeigt worden. Die Konzentration wird einerseits durch die Dosis bestimmt, andererseits – bei Dauertherapie – auch durch die Kapazität des Organismus, sich des Arzneimittels zu entledigen (Abbildung 3). Letzteres, die Clearance, ist von Individuum zu Individuum oft sehr unterschiedlich und nicht ohne Weiteres vorhersehbar. Plasmakonzentrationsbestimmungen im Rahmen des sogenannten Therapeutischen Drug Monitoring (TDM) können unter bestimmten Voraussetzungen die Therapie unterstützen. Ziel des TDM ist, die Variabilität der DosisWirkungs-Beziehung zu berücksichtigen und zu ermöglichen, durch eine Dosisanpassung individuell auszugleichen. Denn in der Regel gilt: Die Konzentrations-WirkungsBeziehung ist weniger variabel und somit besser vorhersehbar als die Dosis-Wirkungs-Beziehung. Die wichtigsten Gründe für TDM sind: ■ Abklärung eines unerwarteten Therapieversagens, das
heisst, der Patient spricht nicht auf das Arzneimittel an, obwohl dies aufgrund der Dosis und der Behandlungsdauer zu erwarten wäre. ■ Abklärung einer unerwarteten Unverträglichkeit, das heisst, der Patient weist Nebenwirkungen auf, die gewöhnlich erst bei höheren Dosen zu erwarten wären.
Es handelt sich in beiden Fällen also um die Vermutung individuell ungewöhnlicher Dosis-Wirkungs-Beziehungen. Voraussetzung für die Sinnhaftigkeit von TDM ist, dass therapeutische Plasmakonzentrationen für das betreffende Arzneimittel definiert sind. Man spricht vom sogenannten «therapeutischen Bereich». Ein therapeutischer Bereich ist für einige Antidepressiva gut etabliert, für andere wiederum nicht. Denn die Beziehung zwischen
Konzentration und Wirkung ist bei einzelnen Arzneimitteln unterschiedlich eng und unterschiedlich gut untersucht. Der therapeutische Bereich ist dadurch gekennzeichnet, dass bei diesen Arzneimittel-Plasmakonzentrationen in diesem Fenster üblicherweise mit einer therapeutisch erwünschten Wirkung und (noch) nicht mit Nebenwirkungen zu rechnen ist. Gleichwohl gibt es Patienten, die mit einer Plasmakonzentration unterhalb des therapeutischen Bereichs eine ausreichende Wirkung haben, und andere Patienten, die trotz einer therapeutischen Plasmakonzentration bereits Nebenwirkungen (z.B. anticholinerge) verspüren. Plasmakonzentrationen können daher nur mit Einbeziehung der therapeutischen Situation sinnvoll interpretiert werden. Die Konzentrationen allein sind zu wenig aussagekräftig, und von «Normwerten» kann bei Arzneimitteln nicht in dem Sinne gesprochen werden, wie wir das von Konzentrationen körpereigener Stoffe kennen. Wichtig sind folgende Fragen: Wie ist das therapeutische Ansprechen? Sind Nebenwirkungen vorhanden? Welche Dosis ist eingenommen worden und wie lange? Welche Begleiterkrankungen und Begleitmedikationen liegen vor?
Der dritte Fallstrick: Beim thera-
peutischen Drug Monitoring sollen
nicht nur die Konzentrationswerte
allein, sondern die gesamte klinische
Situation berücksichtigt werden.
Die unterschiedlichen Empfehlungsgrade für TDM-Sinnhaftigkeit wurden von der Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie (AGNP) erarbeitet und zusammen mit den empfohlenen therapeutischen Bereichen dargestellt (4). Die dort mit den Empfehlungsgraden 1 («stark empfohlen») beziehungsweise 2 («empfohlen») aufgeführten Antidepressiva sind: ■ Amitriptylin + Nortriptylin ■ Nortriptylin ■ Clomipramin + Desmethylclomipramin ■ Imipramin + Desipramin ■ Desipramin ■ Venlafaxin + O-Desmethylvenlafaxin.
Wenn ein wichtiger Metabolit pharmakologisch aktiv ist, sollte dessen Konzentration mit erfasst werden. Deshalb sollen zum Beispiel unter Amitriptylintherapie sowohl Amitriptylin als auch Nortriptylin bestimmt werden. Für zahlreiche Antidepressiva ist die KonzentrationsWirkungs-Beziehung bis anhin nicht ausreichend geklärt. Der Wert einer Plasmakonzentrationsbestimmung ist dann geringer. Die ungewöhnlichen Dosis-Wirkungs-Beziehungen können auf ungewöhnlichen Dosis-Konzentrations-Beziehungen
Psychiatrie 1•2008
Fortbildung
Unter bestimmten Voraus-
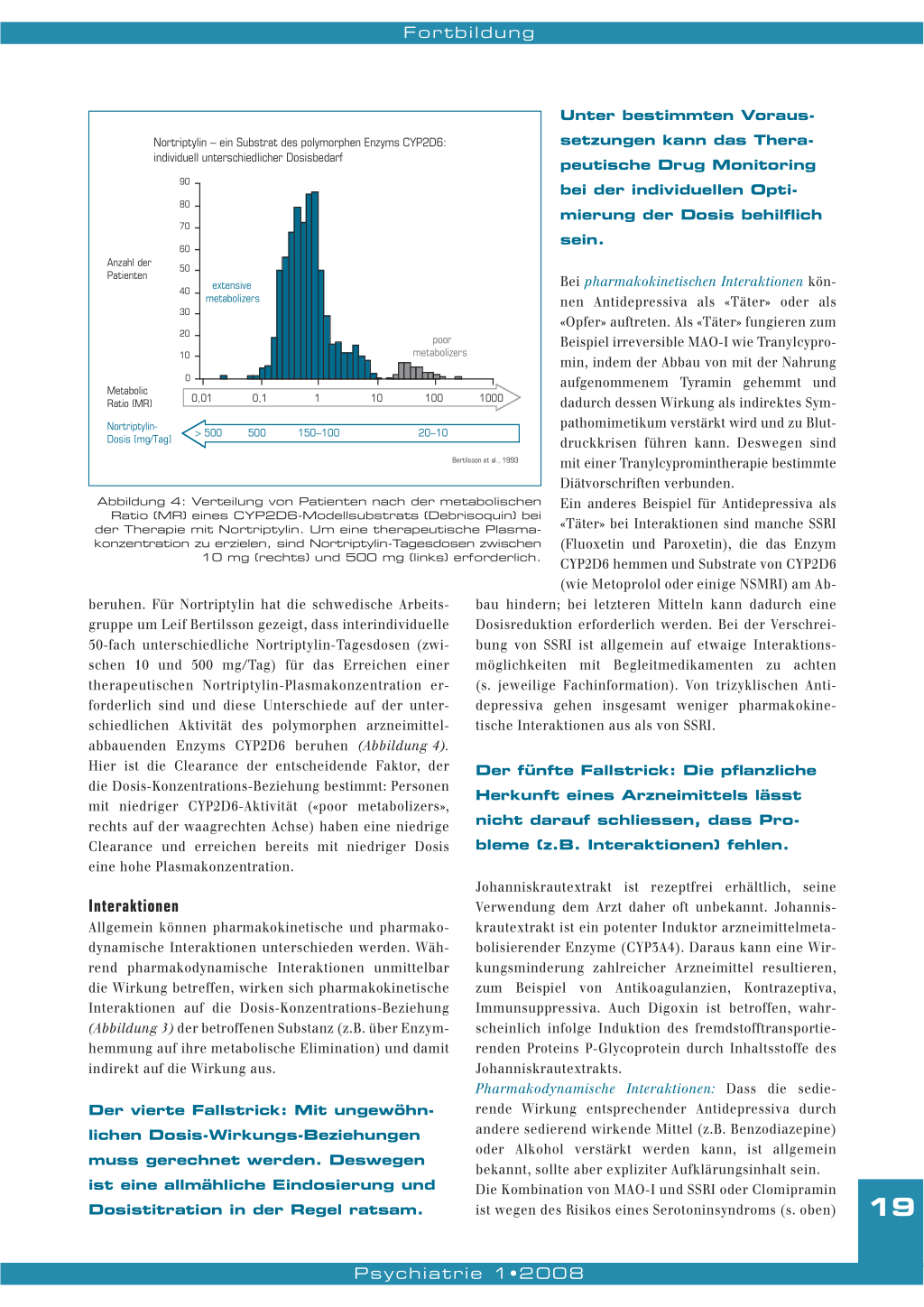
Nortriptylin – ein Substrat des polymorphen Enzyms CYP2D6: individuell unterschiedlicher Dosisbedarf
setzungen kann das Therapeutische Drug Monitoring
Anzahl der Patienten
90
80 70
60 50 40 extensive
metabolizers 30 20 10
poor metabolizers
bei der individuellen Optimierung der Dosis behilflich sein.
Bei pharmakokinetischen Interaktionen können Antidepressiva als «Täter» oder als «Opfer» auftreten. Als «Täter» fungieren zum Beispiel irreversible MAO-I wie Tranylcypromin, indem der Abbau von mit der Nahrung
Metabolic Ratio (MR)
0 0,01
0,1
1
10 100 1000
aufgenommenem Tyramin gehemmt und dadurch dessen Wirkung als indirektes Sym-
NortriptylinDosis [mg/Tag]
> 500
500
150–100
20–10
pathomimetikum verstärkt wird und zu Blutdruckkrisen führen kann. Deswegen sind
Bertilsson et al., 1993
mit einer Tranylcypromintherapie bestimmte
Diätvorschriften verbunden.
Abbildung 4: Verteilung von Patienten nach der metabolischen Ratio (MR) eines CYP2D6-Modellsubstrats (Debrisoquin) bei
der Therapie mit Nortriptylin. Um eine therapeutische Plasmakonzentration zu erzielen, sind Nortriptylin-Tagesdosen zwischen
10 mg (rechts) und 500 mg (links) erforderlich.
Ein anderes Beispiel für Antidepressiva als «Täter» bei Interaktionen sind manche SSRI (Fluoxetin und Paroxetin), die das Enzym CYP2D6 hemmen und Substrate von CYP2D6
(wie Metoprolol oder einige NSMRI) am Ab-
beruhen. Für Nortriptylin hat die schwedische Arbeits- bau hindern; bei letzteren Mitteln kann dadurch eine
gruppe um Leif Bertilsson gezeigt, dass interindividuelle Dosisreduktion erforderlich werden. Bei der Verschrei-
50-fach unterschiedliche Nortriptylin-Tagesdosen (zwi- bung von SSRI ist allgemein auf etwaige Interaktions-
schen 10 und 500 mg/Tag) für das Erreichen einer möglichkeiten mit Begleitmedikamenten zu achten
therapeutischen Nortriptylin-Plasmakonzentration er- (s. jeweilige Fachinformation). Von trizyklischen Anti-
forderlich sind und diese Unterschiede auf der unter- depressiva gehen insgesamt weniger pharmakokine-
schiedlichen Aktivität des polymorphen arzneimittel- tische Interaktionen aus als von SSRI.
abbauenden Enzyms CYP2D6 beruhen (Abbildung 4).
Hier ist die Clearance der entscheidende Faktor, der die Dosis-Konzentrations-Beziehung bestimmt: Personen mit niedriger CYP2D6-Aktivität («poor metabolizers», rechts auf der waagrechten Achse) haben eine niedrige
Der fünfte Fallstrick: Die pflanzliche Herkunft eines Arzneimittels lässt nicht darauf schliessen, dass Pro-
Clearance und erreichen bereits mit niedriger Dosis bleme (z.B. Interaktionen) fehlen.
eine hohe Plasmakonzentration.
Johanniskrautextrakt ist rezeptfrei erhältlich, seine
Interaktionen
Verwendung dem Arzt daher oft unbekannt. Johannis-
Allgemein können pharmakokinetische und pharmako- krautextrakt ist ein potenter Induktor arzneimittelmeta-
dynamische Interaktionen unterschieden werden. Wäh- bolisierender Enzyme (CYP3A4). Daraus kann eine Wir-
rend pharmakodynamische Interaktionen unmittelbar kungsminderung zahlreicher Arzneimittel resultieren,
die Wirkung betreffen, wirken sich pharmakokinetische zum Beispiel von Antikoagulanzien, Kontrazeptiva,
Interaktionen auf die Dosis-Konzentrations-Beziehung Immunsuppressiva. Auch Digoxin ist betroffen, wahr-
(Abbildung 3) der betroffenen Substanz (z.B. über Enzym- scheinlich infolge Induktion des fremdstofftransportie-
hemmung auf ihre metabolische Elimination) und damit renden Proteins P-Glycoprotein durch Inhaltsstoffe des
indirekt auf die Wirkung aus.
Johanniskrautextrakts.
Pharmakodynamische Interaktionen: Dass die sedie-
Der vierte Fallstrick: Mit ungewöhn-
rende Wirkung entsprechender Antidepressiva durch
lichen Dosis-Wirkungs-Beziehungen muss gerechnet werden. Deswegen ist eine allmähliche Eindosierung und
andere sedierend wirkende Mittel (z.B. Benzodiazepine) oder Alkohol verstärkt werden kann, ist allgemein bekannt, sollte aber expliziter Aufklärungsinhalt sein. Die Kombination von MAO-I und SSRI oder Clomipramin
Dosistitration in der Regel ratsam.
ist wegen des Risikos eines Serotoninsyndroms (s. oben)
19
Psychiatrie 1•2008
Fortbildung
kontraindiziert, und beim Umsetzen sind Sicherheitsabstände einzuhalten (Fachinformation). Auch andere Stoffe, die das Serotoninsystem beeinflussen, zum Beispiel die als Migränemittel verwendeten sogenannten Triptane (z.B. Sumatriptan), Johanniskrautextrakt, Serotoninpräkursoren (Tryptophan, Oxitriptan), Sibutramin oder Carbamazepin, sollen deswegen nicht mit SSRI, Venlafaxin oder MAO-I kombiniert werden. Die Kenntnisse zum therapeutischen Einsatz von Antidepressivakombinationen, vor allem zu Sicherheitsfragen, sind bis heute unbefriedigend.
sich rasch entwickelnden Gebiet der Pharmakogenetik
sollen den Weg zu einer individuell massgeschneiderten
Therapie bereiten.
■
Der sechste Fallstrick: Antidepressiva sind nicht beliebig miteinander kombinierbar. Ausserdem können sie bei Interaktionen, auch mit anderen Arzneistoffen, als «Täter» oder «Opfer» fungieren.
Priv.-Doz. Dr. med. Klaus Mörike Universitätsklinikum Tübingen
Institut für Pharmakologie und Toxikologie Abteilung Klinische Pharmakologie Otfried-Müller-Strasse 45 D-72076 Tübingen
20
Ein weiteres Problem: selektive Publikation
Evidenzbasierte Medizin ist insoweit wertvoll, wie die Evidenzbasis vollständig und frei von Verzerrungen ist. Auf eine wichtige Problematik macht eine jüngst publizierte Arbeit im «New England Journal of Medicine» aufmerksam. Von 74 bei der US-amerikanischen Zulassungsbehörde FDA registrierten Antidepressivastudien wurden 31 Prozent aus unbekannten Gründen nicht publiziert. Nach der publizierten Literatur ergaben 94 Prozent der Studien ein positives Ergebnis, dagegen nach FDA-Analyse 51 Prozent (10).
Der siebente Fallstrick:
Es besteht kein Verlass darauf, dass
alle Studien publiziert sind und die
Evidenzbasis frei von Verzerrungen
durch Publikations-Bias ist.
Schlussfolgerung und Ausblick
Angesichts der zahlreichen pharmakodynamischen und pharmakokinetischen Eigenschaften, die einem Arzneimittel zukommen, und der damit verbundenen Fallstricke – einige wurden hier besprochen –, erscheint es sinnvoll, als Therapeut eine persönliche Auswahl aus der grossen Zahl verfügbarer Arzneimittel zu treffen und das eigene Arsenal auf wenige gut vertraute Wirkstoffe zu beschränken. Eine Therapie, die die individuellen Unterschiede im therapeutischen Ansprechen sowie im Risiko für unerwünschte Wirkungen berücksichtigt, ist die Vision für die Zukunft. Bis anhin ist sie nur für vereinzelte Fragestellungen möglich. Erkenntnisse der Forschung auf dem
Interessenkonflikte: keine
Literatur: 1. Arzneimittelkommission der deutschen Ärzteschaft: Empfehlungen
zur Therapie der Depression. 2. Auflg.; Arzneiverordnung in der Praxis 33 Sonderheft 1 (Juli 2006). www.akdae.de. 2. Benkert O, Hippius H: Kompendium der Psychiatrischen Pharmakotherapie. 6. Auflg.; Heidelberg: Springer-Verlag (2007). 3. Arzneimittelkommission der deutschen Ärzteschaft (Hrsg.): Arzneiverordnungen. 21. Auflg.; Köln: Deutscher Ärzte-Verlag (2006). Kapitel 14: Depressionen. 4. Baumann P, Hiemke C, Ulrich S, Eckermann G, Gaertner I, Gerlach M, Kuss H-J, Laux G, Müller-Oerlinghausen B, Rao ML, Riederer P, Zernig G. The AGNP-TDM expert group consensus guidelines: Therapeutic drug monitoring in psychiatry. Pharmacopsychiatry 37, 243–265 (2004). 5. Fick DM, Cooper JW, Wade WE, Waller JL, Maclean JR, Beers MH: Updating the Beers criteria for potentially inappropriate medication use in older adults. Arch Intern Med 163, 2716–2724 (2003). 6. Isbister GK, Buckley NA, Whyte IM: Serotonin toxicity: a practical approach to diagnosis and treatment. Med J Austral 187, 361–365 (2007). 7. Boyer EW, Shannon M: The serotonin syndrome. N Engl J Med 352 (11), 1112–1120 (2005). 8. www.fda.gov/cder/drug/advisory/SSRI_SS200607.htm 9. Khawam EA, Laurencic G, Malone DA: Side effects of antidepressants. An overview. Cleveland Clin J Med 73, 351–361 (2006). 10. Turner EH, Matthews AM, Linardatos E, Tell RA, Rosenthal R: Selective publication of antidepressant trials and its influence on apparent efficacy.
Psychiatrie 1•2008