Transkript
FORSCHUNG
Effektive Behandlung der Rhinosinusitis bei Kindern
Wirksamkeit eines pflanzlichen Präparats
Der vorliegende Artikel ist der
Zweitabdruck des Originalar-
tikels Biebach K., Kramer A.:
Effektive Behandlung der Rhi-
nosinusitus bei Kindern, päd –
Praktische Pädiatrie 2004(10),
333–336. Zweitabdruck mit
freundlicher Genehmigung
der Autorinnen und der Omni-
med-Verlagsgesellschaft mbH.
Einleitung
Infekte der oberen Atemwege zählen zu den häufigsten Erkrankungen im Kindesalter und machen zirka 80 bis 90 Prozent aller Atemwegsinfektionen aus. Vorschulkinder erleiden pro Jahr 5 bis 7 Infektionen der oberen Atemwege (1). Infekte des Hals- und Rachenraums gehören zu den Erkrankungen, die häufig zur Konsultation des Kinder-, Allgemein- oder HNO-Arztes führen. In der Regel werden diese Infekte immer von einer akuten Rhinosinusitis begleitet. Die Ursache hierfür ist unter anderem in den im Vergleich zu Erwachsenen deutlich engeren anatomischen Verhältnissen im Bereich der Nase und Nasennebenhöhlen zu sehen.
Epidemiologie und Pathogenese In der Regel resultiert die akute Rhinosinusitis aus einer primär viralen Infektion (Adeno-, Parainfluenza-, Influenza- und Rhinoviren). Eine Superinfektion der viralen Rhinosinusitis mit Bakterien (Strepto-
coccus pneumoniae, Haemophilus influenza und Moraxella catarrhalis) ist möglich (2). Im Rahmen verschiedener Studien konnte gezeigt werden, dass bei Patienten mit Symptomen einer Rhinosinusitis bis zu einer Krankheitsdauer von sieben Tagen eine bakterielle Infektion unwahrscheinlich ist. Innerhalb der ersten Woche sind lediglich 20 Prozent der Sinusitiden bakteriell bedingt (3) und bis zur vierten Woche 35 Prozent (4). Nach Naumann kommt es aufgrund des viralen Infekts und dem daraus resultierenden entzündungsbedingten Verschluss des Nasennebenhöhlen-Ostiums zu einem Verlust von Ventilation und Drainage, Stagnation des Sekrets, Änderung der Sekretzusammensetzung und Absinken des pH-Werts in den Nasennebenhöhlen (5). Bei Kindern entsteht als Folge einer viralen Rhinosinusitis in 5 bis 10 Prozent der Fälle eine akute bakterielle Rhinosinusitis (6) – im Vergleich dazu bei Erwachsenen nur in 0,2 bis 2 Prozent der viralen Nasennebenhöhlenentzündungen (3).
Klinische Symptomatik Wesentliche Symptome, die auf eine akute Rhinosinusitis hindeuten, jedoch keine Unterscheidung in virale und bakterielle Infektion ermöglichen, sind in Tabelle 1 erwähnt (2). Die Übersichtsarbeit von Wald (6) liefert Anhaltspunkte für die Differenzierung zwischen akuter viraler und akuter bakterieller Rhinosinusitis:
◆ Die meisten unkomplizierten viralen Rhinosinusitiden dauern 5 bis 7 Tage.
◆ Bis zu einer Erkrankungsdauer von 10 Tagen kann eine akute virale Rhinosinusitis zugrunde gelegt werden.
◆ Eine Erkrankungsdauer unter symptomatischer Behandlung von 10 bis 30 Tagen ohne Besserung der Symptomatik deutet auf eine akute bakterielle Rhinosinusitis hin.
◆ Ebenso deutet die Kombination von hohem Fieber und eitrigem Nasensekret über eine Dauer von 3 bis 4 Tagen auf eine sekundäre bakterielle Infektion hin. Diese Kinder klagen oftmals über Kopfschmerzen über oder hinter den Augen und haben sehr selten periorbitale Ödeme (6).
Bei Kindern ist die Symptomatik häufig weniger typisch als bei Erwachsenen; insbesondere bei Kindern im Kleinkindalter kann als einziges Symptom Husten auffallen.
Therapie Zahlreiche Studien sowohl an Erwachsenen als auch an Kindern belegen, dass eine frühzeitige antibiotische Intervention keinen Vorteil gegenüber Plazebo bietet. Dies gilt sowohl hinsichtlich der Symptombefreiung als auch der Prävention von Komplikationen (7–9). Diese wissenschaftliche Erkenntnis sowie die kontinuierliche Zunahme von Antibiotikaresistenzen haben in den letzten Jahren zu einer Neuorientie-
Tabelle 1:
Symptome, die auf eine akute Rhinosinusitis hindeuten, jedoch keine Unterscheidung in virale und bakterielle Infektion ermöglichen
Persistierendes Nasensekret Husten Weitere Symptome
Dünn- oder dickflüssig, klar oder schleimig-eitrig Trocken oder produktiv, tagsüber oder nachts Mundgeruch, schmerzfreies periorbitales Ödem, erhöhte Temperatur oder hohes Fieber > 39 °C
thema6
PHYTOTHERAPIE
3/2010
FORSCHUNG
rung der Therapiestrategie bei akuten Rhinosinusitiden insbesondere bei Kindern geführt (7, 10, 11). Das primäre Therapieziel bei der Behandlung der Rhinosinusitis ist die Wiederherstellung der Sekretdrainage und der Ventilation der Nasennebenhöhlen. Abschwellende Nasentropfen, die ebenfalls häufig bei der Sinusitis verwendet werden, sind zwar effektiv in der Behandlung des Symptoms der verstopften Nase, eine Wirksamkeit bei der Sinusitis ist bislang jedoch nicht nachgewiesen (12). Antihistaminika sind nur bei einer Sinusitis auf Grundlage einer allergischen Rhinitis angezeigt. Für Sinupret® liegen ausgezeichnete Ergebnisse in der Therapie der akuten Rhinosinusitis bei Erwachsenen vor. Dieses vorhandene Datenmaterial sollte nun um die Erfahrungen aus der praktischen Anwendung bei Kindern ergänzt werden.
Ziel der nicht interventionellen Studie
Das pflanzliche Arzneimittel Sinupret® ist seit mehr als 70 Jahren in Deutschland und mittlerweile in mehr als 30 weiteren Ländern zugelassen.* Das Arzneimittel ist «zur Behandlung der akuten und chronischen Sinusitis» bei Kindern und Erwachsenen indiziert. Die fünf enthaltenen Arzneipflanzen (Gentiana lutea, Primula veris, Rumex spec., Sambucus nigra, Verbena officinalis) zeigten in verschiedenen Untersuchungen ein breites Wirkspektrum bei den typischen Symptomen der Rhinosinusitis (13, 14). Basierend auf toxikologischen und klinischen Studien und der langjährigen Vermarktungserfahrung, fällt die NutzenRisiko-Bewertung für das Arzneimittel ausgesprochen positiv aus (15). Um weitere Daten zur Wirksamkeit und Sicherheit von Sinupret® bei Kindern mit Sinusitis zu erhalten, wurde eine multizentrische, nicht interventionelle Studie zur Therapie unter Praxisbedingungen durchgeführt.
Methodik
Die Studie wurde von März 2002 bis September 2003 in 967 ärztlichen Praxen in Deutschland durchgeführt (Pädiater, Allgemeinmediziner, HNO-Fachärzte). Insgesamt konnten die Daten von 3109 Kindern mit typischen Symptomen einer Sinusitis aus-
* Anm. d. Redaktion: Das Präparat ist unter dem Namen Sinupret auch in der Schweiz zugelassen und wird von der Firma Biomed vertrieben.
gewertet werden. Die Alters- und Geschlechtsverteilung zeigt Tabelle 2, das mittlere Alter betrug 6,9 Jahre. Zwei Drittel (64%) der Kinder erhielten dreimal täglich im Mittel 20 Sinupret®Tropfen, wobei die Dosierung getrennt nach Altersklassen unterschiedlich gewählt wurde. Die übrigen Kinder erhielten dreimal täglich ein Sinupret®-Dragee. Im Verlauf der Behandlungszeit wurde die Anzahl der Tropfen leicht reduziert. Die Dragees wurden vorwiegend bei den älteren Kindern (7–12 Jahre) eingesetzt. Bei 10,3 Prozent der Patienten in der Altersgruppe von 2 bis 6 Jahren kamen – vor allem bei den älteren Kindern – auch Dragees zum Einsatz. Die Aufnahmeuntersuchung erfolgte zum Zeitpunkt t0, eine Kontrollvisite (t1) wurde im Schnitt nach 6 Tagen und die Abschlussuntersuchung (t2) nach durchschnittlich 12 Tagen durchgeführt. Die Daten von 523 Kindern < 2 Jahre beziehungsweise > 12 Jahre wurden gemäss den im Beobachtungsplan festgelegten Alterskriterien nicht in die Auswertung aufgenommen. Folgende Symptome wurden bei der Aufnahme- und den Folgeuntersuchungen dokumentiert: ◆ Gesichts-/Kopfschmerz ◆ nasopharyngeales Sekret ◆ behinderte Nasenatmung ◆ Heiserkeit ◆ Husten. Die Veränderung im Vergleich zum Ausgangsbefund und die globale Bewertung der Wirksamkeit und Verträglichkeit durch den Arzt wurden statistisch ausgewertet.
Ergebnisse
Die am häufigsten dokumentierten Symptome bei der Aufnahmeuntersuchung waren das Vorhandensein von NasenRachen-Sekret und die behinderte Nasenatmung: Annähernd alle Kinder (3011 von 3109) berichteten über «viel» (67%) oder
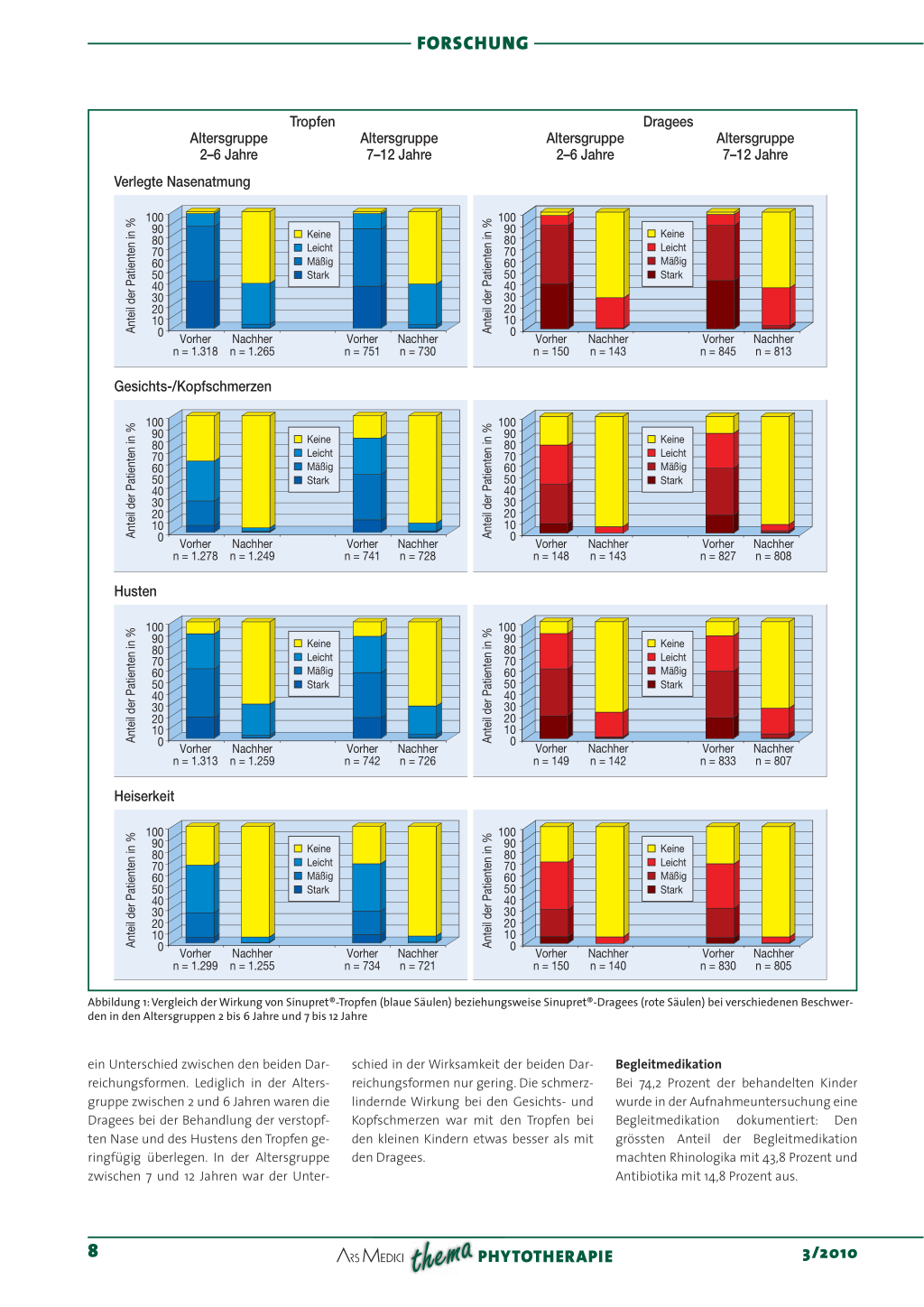
«wenig» (33%) Nasen-Rachen-Sekret von «zäher» (83%) beziehungsweise «dünnflüssiger» (17%) Konsistenz. 71 Prozent beschrieben das Sekret als «gefärbt», nur 29 Prozent als «klar». Behinderte Nasenatmung wurde bei etwa 98 Prozent der Kinder in beiden Altersklassen beschrieben. Der Anteil an Kindern mit schwerer Beeinträchtigung der Nasenatmung betrug in beiden Altersklassen etwa 40 Prozent. Husten war mit 90 beziehungsweise 88 Prozent das am zweithäufigsten genannte Symptom. 60 beziehungsweise 57 Prozent der Kinder klagten über schweren oder mittelschweren Husten. 62,5 beziehungsweise 83,5 Prozent der Kinder berichteten über Gesichts- beziehungsweise Kopfschmerz. Etwa 68 Prozent der Kinder berichteten über Heiserkeit, die in der Mehrheit der Fälle nur gering ausgeprägt war (zusammengefasst in Abbildung 1).
Abschlussbefunde Bei der Abschlussuntersuchung berichteten 93 Prozent der Patienten über «wenig» Sekret, oder bei ihnen wurde keine relevante Menge an Nasen-Rachen-Sekret dokumentiert. Die Konsistenz des noch vorhandenen Sekrets war in über 90 Prozent «dünnflüssig» und «klar». Am Ende der Behandlung hatten nur noch zirka 0,3 Prozent der Kinder eine schwerwiegende Behinderung der Nasenatmung, weniger als 3 Prozent eine mittelgradig verstopfte Nase. Auch bei der Symptomatik «Husten» war eine deutliche Besserung zu beobachten: Am Ende der Studie hatten zirka 75 Prozent der Kinder keinen Husten mehr, die restlichen hatten mehrheitlich nur noch leichten Husten. Ohne Kopfschmerzen waren nach Therapieende 96 beziehungsweise 92 Prozent. Nur zirka 5 Prozent der Kinder berichteten noch über leichte Heiserkeit (zusammengefasst in Abbildung 1 und Tabelle 3). Bei der Beurteilung der Wirksamkeit von Tropfen und Dragees auf die dokumentierten Symptome zeigte sich kaum
Tabelle 2:
Alters- und Geschlechtsverteilung in der multizentrischen, nicht interventionellen Studie
Gesamt Altersgruppe 1 (2–6 Jahre) Altersgruppe 2 (7–12 Jahre)
Mädchen (n) 1638 759 879
Jungen (n) 1471 734 737
Gesamt (n) 3109 1493 1616
3/2010
thema PHYTOTHERAPIE
7
FORSCHUNG
Altersgruppe 2–6 Jahre
Verlegte Nasenatmung
Tropfen
Altersgruppe 7–12 Jahre
Dragees Altersgruppe
2–6 Jahre
Altersgruppe 7–12 Jahre
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher
n = 1.318
Nachher n = 1.265
Gesichts-/Kopfschmerzen
Keine Leicht Mäßig Stark
Vorher Nachher n = 751 n = 730
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher Nachher
n = 150 n = 143
Keine Leicht Mäßig Stark
Vorher Nachher n = 845 n = 813
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher
n = 1.278
Nachher n = 1.249
Husten
Keine Leicht Mäßig Stark
Vorher Nachher n = 741 n = 728
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher Nachher
n = 148 n = 143
Keine Leicht Mäßig Stark
Vorher Nachher n = 827 n = 808
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher
n = 1.313
Nachher n = 1.259
Heiserkeit
Keine Leicht Mäßig Stark
Vorher Nachher n = 742 n = 726
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher Nachher
n = 149 n = 142
Keine Leicht Mäßig Stark
Vorher Nachher n = 833 n = 807
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher
n = 1.299
Nachher n = 1.255
Keine Leicht Mäßig Stark
Vorher Nachher n = 734 n = 721
Anteil der Patienten in %
100 90 80 70 60 50 40 30 20 10 0 Vorher Nachher
n = 150 n = 140
Keine Leicht Mäßig Stark
Vorher Nachher n = 830 n = 805
Abbildung 1: Vergleich der Wirkung von Sinupret®-Tropfen (blaue Säulen) beziehungsweise Sinupret®-Dragees (rote Säulen) bei verschiedenen Beschwerden in den Altersgruppen 2 bis 6 Jahre und 7 bis 12 Jahre
ein Unterschied zwischen den beiden Darreichungsformen. Lediglich in der Altersgruppe zwischen 2 und 6 Jahren waren die Dragees bei der Behandlung der verstopften Nase und des Hustens den Tropfen geringfügig überlegen. In der Altersgruppe zwischen 7 und 12 Jahren war der Unter-
schied in der Wirksamkeit der beiden Darreichungsformen nur gering. Die schmerzlindernde Wirkung bei den Gesichts- und Kopfschmerzen war mit den Tropfen bei den kleinen Kindern etwas besser als mit den Dragees.
Begleitmedikation Bei 74,2 Prozent der behandelten Kinder wurde in der Aufnahmeuntersuchung eine Begleitmedikation dokumentiert: Den grössten Anteil der Begleitmedikation machten Rhinologika mit 43,8 Prozent und Antibiotika mit 14,8 Prozent aus.
thema8
PHYTOTHERAPIE
3/2010
FORSCHUNG
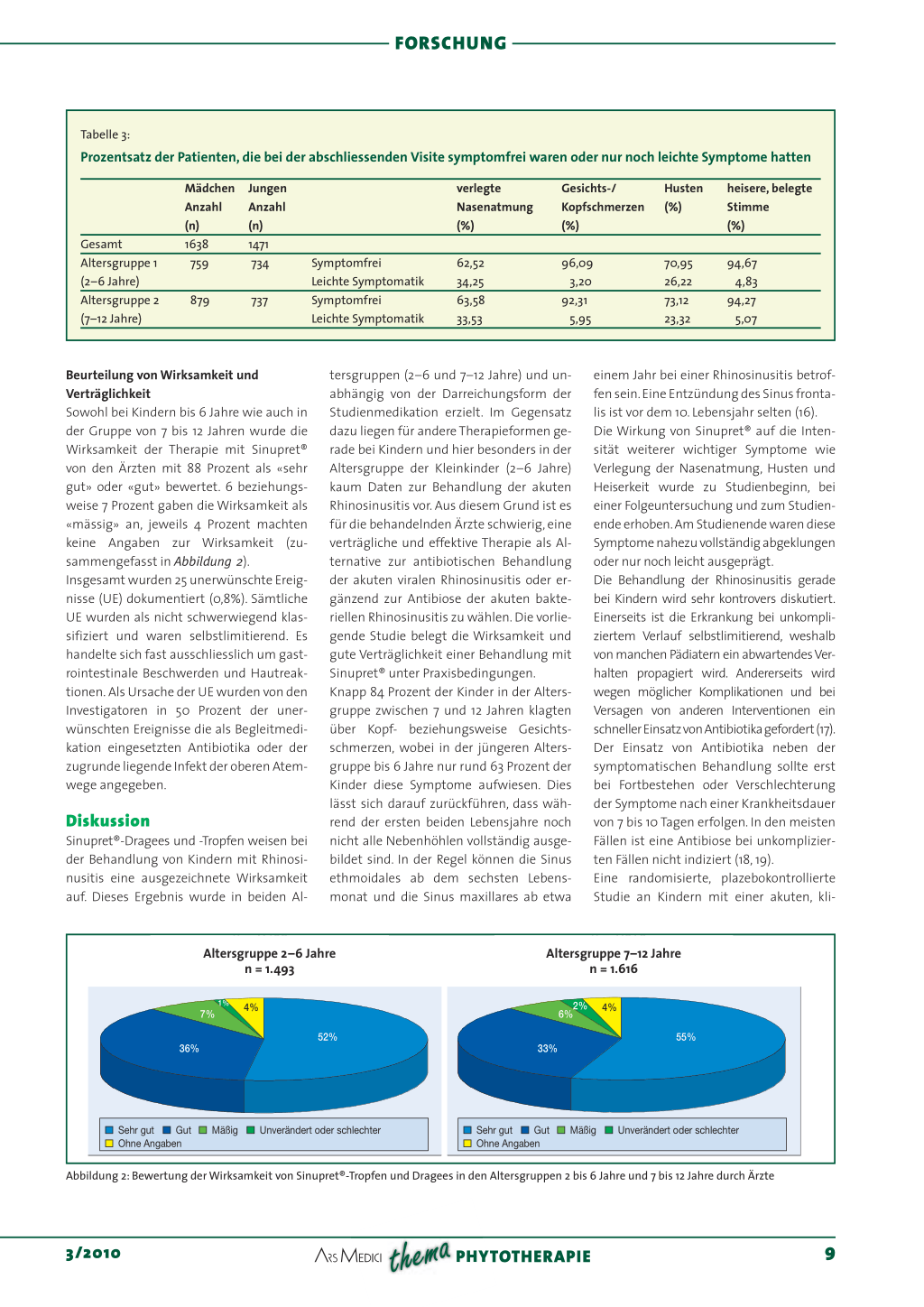
Tabelle 3: Prozentsatz der Patienten, die bei der abschliessenden Visite symptomfrei waren oder nur noch leichte Symptome hatten
Gesamt Altersgruppe 1 (2–6 Jahre) Altersgruppe 2 (7–12 Jahre)
Mädchen Anzahl (n) 1638 759
Jungen Anzahl (n) 1471 734
879 737
Symptomfrei Leichte Symptomatik Symptomfrei Leichte Symptomatik
verlegte Nasenatmung (%)
Gesichts-/ Kopfschmerzen (%)
Husten (%)
heisere, belegte Stimme (%)
62,52 34,25 63,58 33,53
96,09 3,20
92,31 5,95
70,95 26,22 73,12 23,32
94,67 4,83
94,27 5,07
Beurteilung von Wirksamkeit und Verträglichkeit Sowohl bei Kindern bis 6 Jahre wie auch in der Gruppe von 7 bis 12 Jahren wurde die Wirksamkeit der Therapie mit Sinupret® von den Ärzten mit 88 Prozent als «sehr gut» oder «gut» bewertet. 6 beziehungsweise 7 Prozent gaben die Wirksamkeit als «mässig» an, jeweils 4 Prozent machten keine Angaben zur Wirksamkeit (zusammengefasst in Abbildung 2). Insgesamt wurden 25 unerwünschte Ereignisse (UE) dokumentiert (0,8%). Sämtliche UE wurden als nicht schwerwiegend klassifiziert und waren selbstlimitierend. Es handelte sich fast ausschliesslich um gastrointestinale Beschwerden und Hautreaktionen. Als Ursache der UE wurden von den Investigatoren in 50 Prozent der unerwünschten Ereignisse die als Begleitmedikation eingesetzten Antibiotika oder der zugrunde liegende Infekt der oberen Atemwege angegeben.
Diskussion
Sinupret®-Dragees und -Tropfen weisen bei der Behandlung von Kindern mit Rhinosinusitis eine ausgezeichnete Wirksamkeit auf. Dieses Ergebnis wurde in beiden Al-
tersgruppen (2–6 und 7–12 Jahre) und unabhängig von der Darreichungsform der Studienmedikation erzielt. Im Gegensatz dazu liegen für andere Therapieformen gerade bei Kindern und hier besonders in der Altersgruppe der Kleinkinder (2–6 Jahre) kaum Daten zur Behandlung der akuten Rhinosinusitis vor. Aus diesem Grund ist es für die behandelnden Ärzte schwierig, eine verträgliche und effektive Therapie als Alternative zur antibiotischen Behandlung der akuten viralen Rhinosinusitis oder ergänzend zur Antibiose der akuten bakteriellen Rhinosinusitis zu wählen. Die vorliegende Studie belegt die Wirksamkeit und gute Verträglichkeit einer Behandlung mit Sinupret® unter Praxisbedingungen. Knapp 84 Prozent der Kinder in der Altersgruppe zwischen 7 und 12 Jahren klagten über Kopf- beziehungsweise Gesichtsschmerzen, wobei in der jüngeren Altersgruppe bis 6 Jahre nur rund 63 Prozent der Kinder diese Symptome aufwiesen. Dies lässt sich darauf zurückführen, dass während der ersten beiden Lebensjahre noch nicht alle Nebenhöhlen vollständig ausgebildet sind. In der Regel können die Sinus ethmoidales ab dem sechsten Lebensmonat und die Sinus maxillares ab etwa
einem Jahr bei einer Rhinosinusitis betroffen sein. Eine Entzündung des Sinus frontalis ist vor dem 10. Lebensjahr selten (16). Die Wirkung von Sinupret® auf die Intensität weiterer wichtiger Symptome wie Verlegung der Nasenatmung, Husten und Heiserkeit wurde zu Studienbeginn, bei einer Folgeuntersuchung und zum Studienende erhoben. Am Studienende waren diese Symptome nahezu vollständig abgeklungen oder nur noch leicht ausgeprägt. Die Behandlung der Rhinosinusitis gerade bei Kindern wird sehr kontrovers diskutiert. Einerseits ist die Erkrankung bei unkompliziertem Verlauf selbstlimitierend, weshalb von manchen Pädiatern ein abwartendes Verhalten propagiert wird. Andererseits wird wegen möglicher Komplikationen und bei Versagen von anderen Interventionen ein schneller Einsatz von Antibiotika gefordert (17). Der Einsatz von Antibiotika neben der symptomatischen Behandlung sollte erst bei Fortbestehen oder Verschlechterung der Symptome nach einer Krankheitsdauer von 7 bis 10 Tagen erfolgen. In den meisten Fällen ist eine Antibiose bei unkomplizierten Fällen nicht indiziert (18, 19). Eine randomisierte, plazebokontrollierte Studie an Kindern mit einer akuten, kli-
n = 1.493
Altersgruppe 2–6 Jahre n = 1.493
n = 1.616
Altersgruppe 7–12 Jahre n = 1.616
1%
7%
4%
36%
52%
2% 6%
4%
33%
55%
Sehr gut Gut Ohne Angaben
Mäßig
Unverändert oder schlechter
Sehr gut Gut Ohne Angaben
Mäßig
Unverändert oder schlechter
Abbildung 2: Bewertung der Wirksamkeit von Sinupret®-Tropfen und Dragees in den Altersgruppen 2 bis 6 Jahre und 7 bis 12 Jahre durch Ärzte
3/2010
thema PHYTOTHERAPIE
9
FORSCHUNG
nisch diagnostizierten Sinusitis zeigte, dass gegenüber der Plazebogruppe kein klinischer Vorteil zu erzielen war, wenn die Kinder mit Antibiotika behandelt wurden. Weder die Symptome wurden gebessert noch die Symptomdauer verkürzt. Auch die Fehltage in Schule oder Kindergarten wurden nicht reduziert. In keiner der Gruppen traten innerhalb der zweimonatigen Nachbeobachtungszeit Komplikationen auf. Die Autoren folgern, dass die Gabe von Antibiotika drei Wochen nach dem Auftreten der Symptome ausreichend ist und damit der unnötige Einsatz von Antibiotika deutlich reduziert werden könnte (7). Bei Kindern sind Streptococcus pneumoniae, Haemophilus influenzae und Moraxella catarrhalis die Leitkeime der bakteriellen Superinfektion einer Rhinosinusitis, ähnlich wie bei Erwachsenen, jedoch in einer anderen Häufigkeitsverteilung (4, 20, 21). Die Analyse nasopharyngealer Kulturen von Kindern mit akuter Maxillarsinusitis und Maxillarsinusitis-Rezidiven zeigte einen hohen Anteil an Resistenzen der Leitkeime Streptococcus pneumoniae und Haemophilus influenzae bei den rezidivierenden Sinusitiden gegenüber den gebräuchlichen Antibiotika (22). Vorrangiges Therapieziel bei der Behandlung der akuten Rhinosinusitis sollte die Wiederherstellung der Belüftung und Drainage sein, um rasch Beschwerden zu lindern und Komplikationen zu vermeiden. Ein breites Wirkspektrum zur Behandlung der unterschiedlichen Symptome der Rhinosinusitis bietet das pflanzliche Kombinationspräparat Sinupret®. In der vorliegenden Studie wurde die Wirksamkeit von den teilnehmenden Ärzten sehr positiv beurteilt.Zudem wurde die Verträglichkeit von Sinupret® als ausgesprochen gut eingeschätzt. Die verschiedenen Pflanzeninhaltsstoffe des Phytopharmakons haben sekretolytische, antiphlogistische, antivirale und immunmodulierende Wirkung, sodass alle Symptome und Ursachen der Rhinosinusitis behandelt werden können (Tabelle 4).
Zusammenfassung
Die erste nichtinterventionelle Studie mit Sinupret® bei Kindern bestätigt die aus klinischen Studien bekannte gute Wirksamkeit und Verträglichkeit des pflanzlichen Kombinationspräparates bei akuter Sinusitis. Aufgrund des breiten Wirkspektrums stehen mit den Darreichungsformen Tropfen und Dragees schonende Therapeutika
Tabelle 4: Wirkspektrum der Pflanzeninhaltsstoffe in Sinupret®
Enzianwurzel Gentiana lutea Primelblüten Primula veris Eisenkraut Verbena officinalis Holunderblüten Sambucus nigra Ampferkraut Rumex spec.
Sekretolytisch X
X
X
X
X
Antiphlogistisch
X (X)* (X)* X
* Aufgrund des hohen Flavonoidgehalts wahrscheinlich
Antiviral
X X
Immunmodulierend
X
zur Behandlung einer Rhinosinusitis bei
Kindern ab zwei Jahren zur Verfügung. Das
Spektrum der dokumentierten uner-
wünschten Ereignisse beziehungsweise
unerwünschten Arzneimittelwirkungen
unterscheidet sich nicht von dem der Er-
wachsenen. Es wurden keine neuen
Nebenwirkungen identifiziert. Die Häufig-
keit der dokumentierten unerwünschten
Ereignisse liegt deutlich unter 1 Prozent.
Damit bestätigt die vorliegende Studie er-
neut die Wirksamkeit und gute Verträglich-
keit von Sinupret® in der Therapie der aku-
ten Rhinosinusitis bei Kindern.
◆
Anschrift für die Verfasser: Dr. med. Katrin Biebach Schloss-Prunn-Strasse 1 D-81375 München
Literatur:
1. Roncevic N et al. (2002): Treatment of acute upper respiratory tract infections in children. Med Pregl 55 (9–10), 397–400.
2. Isaacs D (1996): Clinical Spectrum of Disease in Children. In: Myint S, Taylor-Robinson D (eds): Viral and other infections of the human respiratory tract. Chapman & Hall, 47–60.
3. Hickner JM et al. (2001): Principles of appropriate antibiotic use for acute rhinosinusitis in adults: Background. Ann Intern Med 134, 498–505.
4. Hansen et al. (1995): Predicting acute maxillary sinusitis in a general practice population. BMJ 311, 233–236.
5. Naumann HH (1966): Pathologische Anatomie der chronischen Rhinitis und Sinusitis; Int. Congress of Internal Medicine 113, 79– 87, 196.
6. Wald ER (1998): Sinusitis. Pediatr Ann 27, 811–818.
7. Garbutt JM et al. (2001): A randomized, placebocontrolled trial of antimicrobial treatment for children with clinically diagnosed acute sinusitis. Pediatrics 107 (4), 619–625.
8. Arroll B, Kenealy T (2004): Antibiotics for the common cold and acute purulent rhinitis (Cochrane Review). In: The Cochrane Library, Issue 3. John Wiley & Sons Ltd, Chichester, UK.
9. Fahey T et al. (1998):Systematic review of the treatment of upper respiratory tract infection. Archiv Dis Child 79, 225–230.
10. Van Buchem FL et al. (1997): Primary-carebased randomised placebo-controlled trial of antibiotic treatment in acute maxilliary sinusitis. The Lancet 349, 683–687.
11. Brink AJ et al. (2004): Guideline for the management of upper respiratory tract infections. S Afr Med J 94 (6 Pt 2), 475–483.
12. Bachert C et al. (2003): An update on the diagnosis and treatment of sinusitis and nasal polyposis. Allergy 58, 176–191.
13. Neubauer N, März RW (1994): Placebo-controlled, randomized double-blind clinical trial with Sinupret sugar-coated tablets on the basis of a therapy with antibiotics and decongestant nasal drops in acute sinusitis. Phytomedicine 1 (3), 177–181.
14. Richstein A, Mann W (1980): Zur Behandlung der chronischen Sinusitis mit Sinupret. Therapie der Gegenwart 119, 1055–1060.
15. März RW et al. (1999): Wirkprofil und Wirksamkeit eines pflanzlichen Kombinationspräparates zur Behandlung der Sinusitis. Wien Med Wochenschr 149 (8–10), 202–208.
16. Pitrez PMC, Pitrez JLB (2003): Acute upper respiratory tract infections – outpatient diagnosis and treatment. J Pediatr (Rio J) 79 Suppl 1, S77–S86.
17. Goldsmith AJ, Rosenfeld RM (2003):Treatment of pediatric sinusitis. Pediatr Clin N Am 50, 413–426.
18. Diagnosis and Treatment of Acute Bacterial Rhinosinusitis. Summary, Evidence Report/Technology Assessment: Number 9 March 1999. Agency for Health Care Policy and Research, Rockville, MD. http://www.ahrq. gov/clinic/epcsums/sinussum.htm.
19. Theis J, Oubichon T (2003): Are antibiotics helpful for acute maxillary sinusitis? J Fam Pract 52 (6), 490–492.
20. van Buchem FL et al. (1995): Acute maxillary sinusitis in general practice: the relation between clinical picture and objective findings. Eur J Gen Pract 1, 155–160.
21. Anon JB (2003): Acute bacterial rhinosinusitis in pediatric medicine: current issues in diagnosis and management. Paediatr Drugs 5 Suppl 1, 25–33.
22. Brook I, Gober AE (2004): Antimicrobial resistance in the nasopharyngeal flora of children with acute maxillary sinusitis and maxillary sinusitis recurring after amoxicillin therapy. J Antimicrob Chemother 53 (2), 399–402 Epub.
thema10
PHYTOTHERAPIE
3/2010