Transkript
FORTBILDUNG
Omega-3-Fettsäuren
Entweder regelmässig fettreichen Fisch essen oder Fischölkapseln schlucken
Heute ist für die meisten Menschen hierzulande die
Zufuhr mit Eicosapentaensäure (EPA) und Docoshexaen-
säure (DHA) tief. Gute natürliche Quellen sind
Meeresfrüchte, vor allem fettreiche Fische. Alternativ
kann zum Erlangen eines optimalen Gesundheits-
zustands und zur Prävention von Krankheiten mit Fisch-
ölkapseln substituiert werden.
PHILIP C. CALDER*
Struktur, Nomenklatur und metabolische Beziehungen der Omega-3-Fettsäuren Fettsäuren sind Kohlenwasserstoffketten mit einer Carboxylgruppe am einen und einer Methylgruppe am anderen Ende. Die Carboxylgruppe ist reaktiv und bildet leicht Esterverbindungen mit alkoholischen Gruppen, beispielsweise mit Glykol oder Cholesterin, was zu Acylglycerolen (z.B. Triacylglycerole, Phospholipide) und Cholesterylestern führt. Die Länge der Fettsäureketten kann zwischen 2 und mehr als 30 betragen, und innerhalb der Kette können Doppelbindungen vorkommen. Fettsäuren mit Doppelbindungen werden als ungesättigte Fettsäuren bezeichnet. Eine Fettsäure mit zwei oder mehr Doppelbindungen wird mehrfach ungesättigt genannt. Fettsäuren tragen gebräuchliche Namen und systematische Bezeichnungen. Sie werden auch in einer Kurznomenklatur angeführt, die die Anzahl der Kohlenstoffatome in der Kette, die Zahl der Doppelbindungen sowie die Stellung der ersten Doppelbindung bezüglich der Methylgruppe (ω [= Omega]; manchmal auch n genannt) angibt. Omega-3-Fettsäuren werden so genannt, weil ihre erste Doppelbindung beim C-Atom Nummer 3 liegt, wobei das Methyl-C als Nummer 1 gerechnet wird. Die einfachste Omega-3-Fettsäure ist die α-(= alpha-)Linolensäure (18:3ω-3). Die α-Linolensäure wird aus der Linolsäure (18:2ω-6) durch eine mittels Delta-15-Desaturase katalysierte Desaturierung gebildet (verwirrenderweise werden die Desa-
turasen nach dem ersten C-Atom, das die eingefügte Doppelbindung trägt, bezeichnet, wobei aber das Carboxyl-C als Nummer 1 gerechnet wird). Tiere inklusive Menschen besitzen das Delta-15-Desaturase-Enzym nicht und sind daher zur α-Linolensäure-Synthese nicht in der Lage. Pflanzen hingegen besitzen dieses Enzym und können so α-Linolensäure bilden. Obwohl Tiere die α-Linolensäure nicht zu synthetisieren vermögen, können sie diese durch weitere Desaturierung und Verlängerung der Kette metabolisieren. Die Desaturierung erfolgt an C-Atomen unterhalb von C-Atom Nummer 9 (vom Carboxyl-C her gezählt) und geschieht vor allem in der Leber. α-Linolensäure kann durch die Delta-6-Desaturase in Stearidonsäure (18:4ω-3) umgewandelt und diese zu 20:4ω-3 elongiert werden (Abbildung 1). Diese Fettsäure kann durch Delta5-Desaturase weiter zur Eicosapentaensäure (20:5ω-3; bekannt als EPA) desaturiert werden (Abbildung 1). Es gibt auch einen Stoffwechselweg zur weiteren Umbildung von EPA in
Merksätze
■ Sehr langkettige Omega-3-Fettsäuren werden leicht und weitgehend dosisabhängig in die Transportspeicher (Blutlipide) sowie die funktionellen (Zellen und Gewebe) und Reservepools (Fettgewebe) eingebaut.
■ Bei ausreichenden Konzentrationen des Einbaus verändern EPA und DHA die physikalische Eigenschaft von Zellmembranen und der membraneiweissvermittelten Reaktionen, die Eicosanoidbildung, die Zellsignale sowie die Genexpression in vielen verschiedenen Zelltypen.
■ In den meisten Fällen stimmen die beobachtbaren Effekte mit Verbesserungen in den Profilen von Biomarkern oder gesundheitsrelevanten Outcomes überein, weshalb sehr langkettige Omega-3Fettsäuren für das Erlangen eines optimalen Gesundheitszustands bedeutsam sind und in der Prävention von Krankheiten eine Rolle spielen.
■ Typische Empfehlungen gelten für eine minimale Zufuhr von Omega-3-Fettsäuren von 0,2 bis 0,65 g/Tag bis zu 1,5 g/Tag zur allgemeinen Gesundheitsförderung sowie von 1 g/Tag zur Herzinfarktprävention und von 2 bis 4 g/Tag zur Triglyzeridsenkung.
*Institute of Human Nutrition, School of Medicine, University of Southampton
ARS MEDICI 4 ■ 2009 159
FORTBILDUNG
Docosahexaensäure (22:6ω-3; bekannt
bietet. Die letzte Schätzung für den
als DHA): Dieser umfasst den Anbau von zwei C-Atomen zur Docosapentaensäure (22:5ω-3; bekannt als DPA), weitere Addition zweier C-Atome zu 24:5ω-3 und Desaturierung zu 24:6ω-3 sowie Translokation von 24:6 vom en-
H3C COOH ␣-Linolenic acid (18:3n-3) ⌬6-desaturase
H3C C00H
Stearidonic acid (18:4n-3)
Fischverzehr bei Erwachsenen in Grossbritannien liegt bei ungefähr 100 g magerem Fisch und zirka 50 Gramm fettreichem Fisch pro Woche (4); ähnliche (und in gewissen Ländern sogar tiefere) Zufuhren sind in anderen Län-
doplasmatischen Retikulum zu Peroxi-
Elongase
dern Nordeuropas, Osteuropas, Nord-
somen, wo zwei C-Atome durch limitierte Betaoxidation entfernt werden, was dann zu DHA führt (1). Kurzzeitstudien mit Isotopen-markierter α-Li-
H3C
20:4n-3
C00H
⌬5-desaturase
amerikas und Australiens zu erwarten. Höher ist der Verzehr von mageren Fischen in südeuropäischen Ländern und von fettreichen Fischen in Japan
nolensäure und Langzeitstudien mit
H3C
C00H
und einigen anderen asiatischen Län-
signifikant erhöhter Zufuhr von α-Linolensäure haben gezeigt, dass die Umwandlung von EPA, DPA und DHA gering ist, wobei nur eine sehr be-
Eicosapentaenoic acid (20:5n-3)
Elongase Elongase ⌬6-desaturase -oxidation
dern. Die durchschnittliche (mittlere) Zufuhr sehr langkettiger Omega-3-Fettsäuren bei Erwachsenen in Grossbritannien, Nord- und Osteuropa, Nord-
grenzte Umwandlung bis hin zu DHA beobachtet werden konnte (2). EPA und DPA können auch aus DHA durch
H3C C00H Docosahexaenoic acid (22:6n-3)
amerika und Australien beträgt ungefähr 0,15 bis 0,25 g/Tag. Allerdings ist die Einnahmeverteilung biphasisch, da
begrenzte Betaoxidation rückkonvertiert werden.
Abbildung 1: Umwandlung von α-Linolensäuren in längerkettige, stärker ungesättigte Omega-3-Fettsäuren
es Menschen gibt, die fettreiche Fische verzehren, und solche, die dies nicht tun; so ergab eine neuere Schätzung
Quellen aus der Ernährung
eine mediane Zufuhr sehr langketti-
und typische Zufuhr von Omega-3-Fettsäuren
ger Omega-3-Fettsäuen bei australischen Erwachsenen von
Grüne Blätter enthalten einen signifikanten Anteil (typischer- 0,03 g/Tag bei einer mittleren Zufuhr von 0,19 mg/Tag (5). Die
weise 55%) ihrer Fettsäuren in Form von α-Linolensäure, aber Aufnahme dürfte in Populationen mit Verzehr grosser Mengen
grüne Blätter sind keine ergiebige Quelle für Fett. Verschiedene fettreicher Fische, wie in Japan, höher und regelmässiger sein
Samen und Samenöle sowie einige Nüsse enthalten signifi- als in Europa, Nordamerika und Australasien.
kante Mengen von α-Linolensäure. So enthalten Leinsamen Das aus dem Fleisch fettreicher oder aus der Leber magerer
und ihr Öl typischerweise 45 bis 55 Prozent der Fettsäuren in Fische gewonnene Öl wird als «Fischöl» bezeichnet und hat die
Form von α-Linolensäure, Sojabohnen dagegen nur 5 bis 10 herausragende Eigenschaft, sehr reich an sehr langkettigen
Prozent. Auch Rapsöl und Baumnüsse enthalten α-Linolen- Omega-3-Fettsäuren zu sein. Da verschiedene fettreiche Fische
säure, ebenso Maisöl, Sonnenblumenöl und Safloröl (Distelöl), unterschiedliche Mengen von Omega-3-Fettsäuren enthalten,
allerdings nur in sehr geringer Konzentration. Unter Erwach- gilt dies auch für die Fischöle. EPA und DHA umfassen etwa
senen in westlichen Ländern beträgt die typische Zufuhr von 30 Prozent der Fettsäuren in einer typischen Aufbereitung von
α-Linolensäure 0,5 bis 2 g/Tag (2, 3). Die häufigste mehrfach Fischöl, was bedeutet, dass eine 1-Gramm-Kapsel ungefähr
ungesättigte Fettsäure in der westlichen Ernährung ist die 0,3 g EPA plus DHA enthält. Hervorzuheben ist ferner, dass
Omega-6-Fettsäure Linolsäure (18:2ω-6), die im Allgemeinen zwischen verschiedenen Fischen und Fischölen nicht nur die
in 5- bis 20-fach höheren Mengen konsumiert wird als die Menge von Omega-3-Fettsäuren, sondern auch der relative
α-Linolensäure (2, 3).
Anteil der einzelnen sehr langkettigen mehrfach ungesättigten
Fische können klassifiziert werden in magere Fische, die Lipide Omega-3-Fettsäuren (EPA, DPA, DHA) schwanken kann. So ist
in der Leber speichern (z.B. Kabeljau), und fettreiche («ölhal- Kabeljauöl reicher an EPA als DHA, während Thunfischöl mehr
tige») Fische, die Lipide im Fleisch einlagern (z.B. Makrelen, DHA als EPA enthält. Fischleberöle enthalten signifikante Men-
Hering, Lachs, Thunfisch). Verglichen mit anderen Nahrungs- gen fettlöslicher Vitamine, vor allem Vitamin A und D. Präpa-
mitteln, sind Fische und Meeresfrüchte gute Quellen für die rate in Kapselform, die Omega-3-Fettsäuren in höheren Kon-
sehr langkettigen Omega-3-Fettsäuren EPA und DHA. Aller- zentrationen als in Standardfischöl enthalten, sind erhältlich.
dings enthalten verschiedene Arten von Fisch unterschiedliche Fischölkapseln enthalten die Fettsäuren gewöhnlich in Form von
Mengen dieser Fettsäuren und auch verschiedene Verhältnisse Triglyzeriden. Anzumerken ist auch, dass Fischölkapseln ziem-
zwischen EPA und DHA. Dies hängt teilweise von Stoffwech- lich hohe Anteile an Palmitinsäure (16:0) und Palmitoleinsäure
selcharakteristika der Fische ab, aber auch von ihrem Futter, (16:1ω-7) sowie auch etwas Arachidonsäure (20:4ω-6) enthal-
der Wassertemperatur, der Jahreszeit und so weiter. Dennoch ten. Ausser den Fischölkapseln, die Omega-3-Fettsäuren als
ist klar, dass eine einzelne Mahlzeit mit magerem Fisch unge- Triglyzeride enthalten, sind Omega-3-Fettsäuren auch in Phos-
fähr 200 bis 300 mg sehr langkettiger Omega-3-Fettsäuren ent- pholipidform (z.B. als Krillöl) und als Äthylester (z.B. im phar-
hält, während eine Mahlzeit mit fettreichem Fisch 1,5 bis 3 g mazeutischen Präparat Omacor®) erhältlich. Kapseln könnten
160 ARS MEDICI 4 ■ 2009
O M E G A-3 - F E T T S Ä U R E N
eindeutig einen signifikanten Beitrag zur Zufuhr sehr langket- nahezu maximale Einlagerung beider Fettsäuren in Serum-
tiger Omega-3-Fettsäuren leisten. Menschen, die wenig oder cholesterylester innerhalb von 30 Tagen nach Beginn der
gar keinen Fisch essen, könnten durch eine einzige Standard- Supplementation erfolgt, während die maximale Aufnahme in
Fischöl-Kapsel ihre tägliche Zufuhr an sehr langkettigen Erythrozyten erst nach 56 bis 182 Tagen zustande kommt.
Omega-3-Fettsäuren zum Beispiel um das Fünffache (und Yaqoob et al. (13) berichteten von einer zeitabhängigen Einla-
mehr) steigern.
gerung von EPA und DHA in mononukleäre Zellen im Blut,
wobei der nahezu maximale Einbau nach 4 Wochen Supple-
Supplementierung mit sehr langkettigen Omega-3- mentation erreicht wurde. Nach Abbruch der Supplementation
Fettsäuren verändert die Fettsäurezusammensetzung kehrte die EPA-Konzentration in den Mononukleären innert
von Plasma, Zellen und Geweben beim Menschen
8 Wochen zum Ausgangswert zurück, während die Zellen
Verschiedene Plasmalipidpools, Zellen und Gewebe haben DHA zurückzuhalten schienen. Dies ist den Befunden von
unterschiedliche, charakteristische Zusammensetzungen von Opp-Snijders et al. (14) ähnlich, die beobachteten, dass der
Fettsäuren. Eine Veränderung der Fettsäureprofile ist nach Erythrozyten-EPA-Gehalt 8 Wochen nach Supplementations-
Ergänzung der Ernährung durch Fischölkapseln vielfach ende zum Ausgangswert zurückkehrte, während DHA erhöht
Beobachtet worden. Studien berichten, dass eine solche blieb. Dieselben Beobachtungen eines Verlusts von EPA und
Supplementation zum Erscheinen von EPA und DHA in einer selektiven Retention von DHA nach Beendigung der
Plasmalipiden, Blutplättchen, Erythrozyten, Leukozyten, Fischölsupplementation sind auch für Blutplättchen gemacht
Kolongewebe, Herzgewebe und sehr wahrscheinlich vielen worden (15). Somit bietet die Literatur eine bedeutende
anderen Zell- und Gewebetypen führt. Der Einbau von EPA Anzahl von Studien, die belegen, dass EPA und DHA bei
und DHA aus Fischölkapseln erfolgt zum Teil auf Kosten mehr- gesteigerter Zufuhr in Blut-, Zell- und Gewebelipiden einge-
fach ungesättigter sehr langkettiger Omega-6-Fettsäuren wie baut werden.
Arachidonsäure und geschieht dosisabhängig. So berichteten
Studien mit einer täglichen Zufuhr von EPA-plus-DHA in Erhöhte Einnahme von sehr langkettigen
Dosierungen von 1 bis 5 g über eine nahezu lineare Beziehung Omega-3-Fettsäuren nützt der Gesundheit
zwischen EPA-Aufnahme und EPA-Gehalt in Plasmaphospho- Ein erhöhter Gehalt an Omega-3-Fettsäuren in Zellen und Ge-
lipiden (6, 7), und Blonk et al. (8) beobachteten lineare Bezie- weben kann die Zellfunktion durch verschiedene Mechanis-
hungen zwischen Zufuhren von EPA und DHA von 1,5, 3 und men beeinflussen, wie Abbildung 2 zeigt. Diese umfassen:
6 g/Tag und den Anteilen dieser Fettsäuren in Plasmaphos- ■ Veränderungen in den physikalischen Membraneigen-
pholipiden. Sanders und Roshanai (9) zeigten einen dosis-
schaften wie Membranzustand («Fluidität») und Schicht-
abhängigen Einbau von EPA und DHA in Plättchenphospho-
anordnung, die ihrerseits die Aktivität der Membran-
lipide bei Männern, die zwischen 1,6 und 6,5 g EPA plus DHA
proteine beeinflussen, zu denen Rezeptoren, Transport-
pro Tag während dreier Wochen einnahmen. In anderen Studien
eiweisse, Ionenkanäle und Signalenzyme gehören
war die Aufnahme von EPA und DHA in Blutneutrophile (10) ■ Effekte auf Signalwege, entweder durch Modifikation der
und von EPA in Plasmaphospholipide und in mononukleäre
Expression, Aktivität oder Avidität von Membranrezep-
Zellen im Blut (11) linear dosisabhängig. In einer eleganten
toren oder durch Modifikation der intrazelluläreren Signal-
Studie, die Dosisantwort und zeitlichen Verlauf über zwölf
transduktionsmechanismen. Als Ergebnis dieser Wirkungen
Monate bei älteren Männern verband, beobachteten Katan et
wird die Aktivierung von Transkriptionsfaktoren verändert
al. (12) die Fettsäurezusammensetzungen von Serumchol-
und die Genexpression modifiziert.
esterylestern, Erythrozyten und Fettgewebe. Diese Unter- ■ Veränderungen im Muster der produzierten Lipidmediato-
suchung bestätigte, dass EPA und DHA in den Pool zirkulie-
ren. Die verschiedenen Mediatoren haben unterschied-
render Lipide und in Erythrozyten eingebaut werden, wenn
liche biologische Aktivitäten und Potenzen.
ihre Zufuhr gesteigert wird. Sie be-
legte zudem den Einbau von EPA und
DHA in Fettgewebe, also einen Speicherpool, bei höherer Zufuhr. Die
Erhöhte Zufuhr von Omega-3-Fettsäuren
Studie brachte aber auch den eindeutigen Beweis, dass die Einlagerung in
veränderte Zusammensetzung von Membranen
verschiedene Pools mit variierenden Raten und in verschiedenem Ausmass (d.h. mit unterschiedlicher Effizienz) erfolgt und mit der Zufuhr
veränderte Struktur und Fluidität von Membranen (Grobstruktur, Lipidrafts,
Acylierung)
verändertes Muster der Eicosanoid-Synthese
veränderte Wege der Signaltransreduktion
veränderte Muster der Genexpression
(zumindest in den untersuchten
Dosen) nicht in einer strikt linearen
veränderte Zellfunktion und Zellantworten
Form zusammenhängt. Die Studie
von Katan et al. (12) zeigte, dass die
Abbildung 2: Übersichtsschema der interagierenden Mechanismen, durch welche Fettsäuren die Zellfunktion beeinflussen könnten
ARS MEDICI 4 ■ 2009 161
FORTBILDUNG
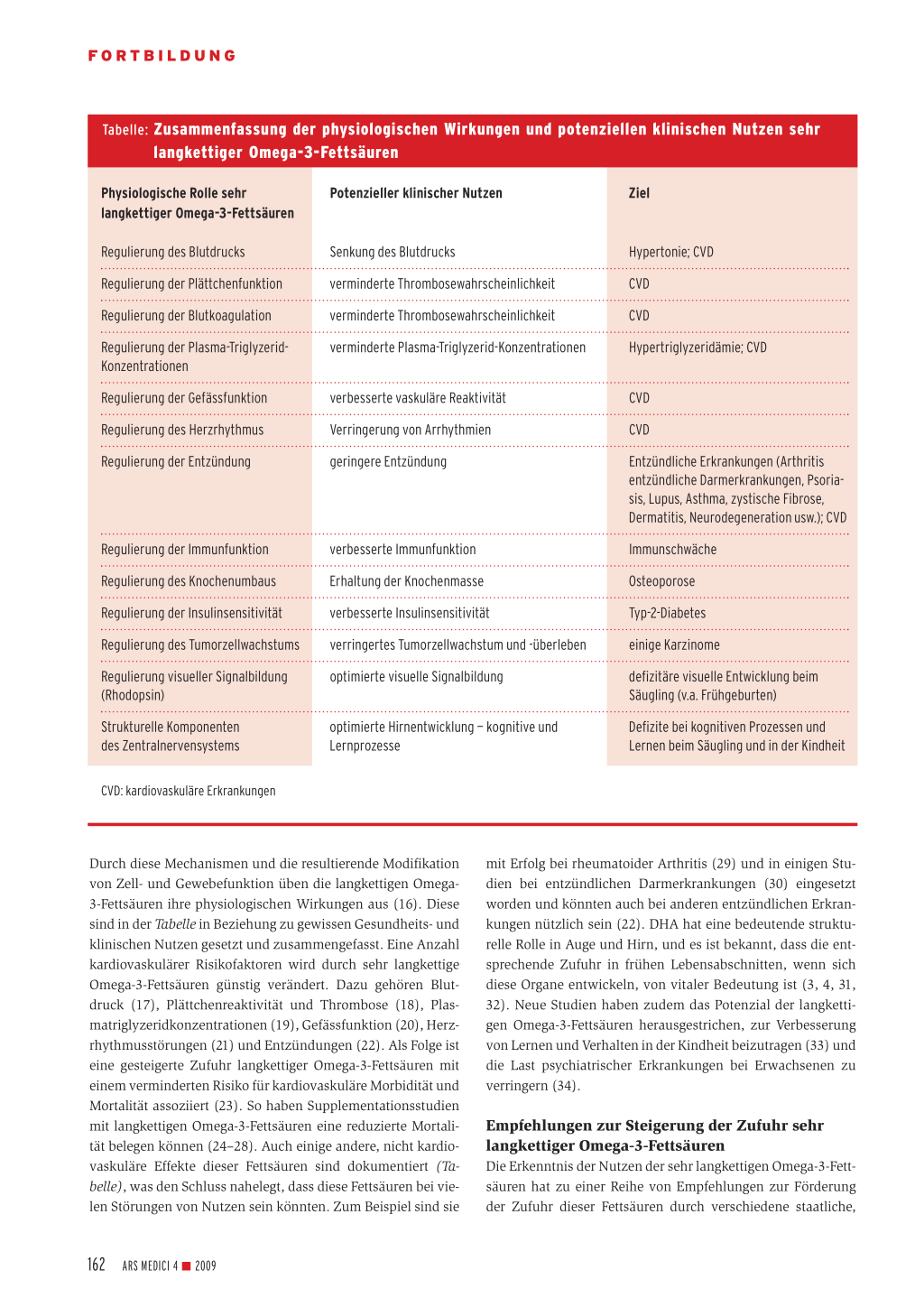
Tabelle: Zusammenfassung der physiologischen Wirkungen und potenziellen klinischen Nutzen sehr Tabelle: langkettiger Omega-3-Fettsäuren
Physiologische Rolle sehr langkettiger Omega-3-Fettsäuren
Potenzieller klinischer Nutzen
Ziel
Regulierung des Blutdrucks Regulierung der Plättchenfunktion Regulierung der Blutkoagulation Regulierung der Plasma-TriglyzeridKonzentrationen Regulierung der Gefässfunktion Regulierung des Herzrhythmus Regulierung der Entzündung
Senkung des Blutdrucks verminderte Thrombosewahrscheinlichkeit verminderte Thrombosewahrscheinlichkeit verminderte Plasma-Triglyzerid-Konzentrationen
verbesserte vaskuläre Reaktivität Verringerung von Arrhythmien geringere Entzündung
Regulierung der Immunfunktion
Regulierung des Knochenumbaus
Regulierung der Insulinsensitivität
Regulierung des Tumorzellwachstums
Regulierung visueller Signalbildung (Rhodopsin)
Strukturelle Komponenten des Zentralnervensystems
verbesserte Immunfunktion Erhaltung der Knochenmasse verbesserte Insulinsensitivität verringertes Tumorzellwachstum und -überleben optimierte visuelle Signalbildung
optimierte Hirnentwicklung — kognitive und Lernprozesse
Hypertonie; CVD CVD CVD Hypertriglyzeridämie; CVD
CVD CVD Entzündliche Erkrankungen (Arthritis entzündliche Darmerkrankungen, Psoriasis, Lupus, Asthma, zystische Fibrose, Dermatitis, Neurodegeneration usw.); CVD Immunschwäche Osteoporose Typ-2-Diabetes einige Karzinome defizitäre visuelle Entwicklung beim Säugling (v.a. Frühgeburten) Defizite bei kognitiven Prozessen und Lernen beim Säugling und in der Kindheit
CVD: kardiovaskuläre Erkrankungen
Durch diese Mechanismen und die resultierende Modifikation von Zell- und Gewebefunktion üben die langkettigen Omega3-Fettsäuren ihre physiologischen Wirkungen aus (16). Diese sind in der Tabelle in Beziehung zu gewissen Gesundheits- und klinischen Nutzen gesetzt und zusammengefasst. Eine Anzahl kardiovaskulärer Risikofaktoren wird durch sehr langkettige Omega-3-Fettsäuren günstig verändert. Dazu gehören Blutdruck (17), Plättchenreaktivität und Thrombose (18), Plasmatriglyzeridkonzentrationen (19), Gefässfunktion (20), Herzrhythmusstörungen (21) und Entzündungen (22). Als Folge ist eine gesteigerte Zufuhr langkettiger Omega-3-Fettsäuren mit einem verminderten Risiko für kardiovaskuläre Morbidität und Mortalität assoziiert (23). So haben Supplementationsstudien mit langkettigen Omega-3-Fettsäuren eine reduzierte Mortalität belegen können (24–28). Auch einige andere, nicht kardiovaskuläre Effekte dieser Fettsäuren sind dokumentiert (Tabelle), was den Schluss nahelegt, dass diese Fettsäuren bei vielen Störungen von Nutzen sein könnten. Zum Beispiel sind sie
mit Erfolg bei rheumatoider Arthritis (29) und in einigen Studien bei entzündlichen Darmerkrankungen (30) eingesetzt worden und könnten auch bei anderen entzündlichen Erkrankungen nützlich sein (22). DHA hat eine bedeutende strukturelle Rolle in Auge und Hirn, und es ist bekannt, dass die entsprechende Zufuhr in frühen Lebensabschnitten, wenn sich diese Organe entwickeln, von vitaler Bedeutung ist (3, 4, 31, 32). Neue Studien haben zudem das Potenzial der langkettigen Omega-3-Fettsäuren herausgestrichen, zur Verbesserung von Lernen und Verhalten in der Kindheit beizutragen (33) und die Last psychiatrischer Erkrankungen bei Erwachsenen zu verringern (34).
Empfehlungen zur Steigerung der Zufuhr sehr langkettiger Omega-3-Fettsäuren Die Erkenntnis der Nutzen der sehr langkettigen Omega-3-Fettsäuren hat zu einer Reihe von Empfehlungen zur Förderung der Zufuhr dieser Fettsäuren durch verschiedene staatliche,
162 ARS MEDICI 4 ■ 2009
FORTBILDUNG
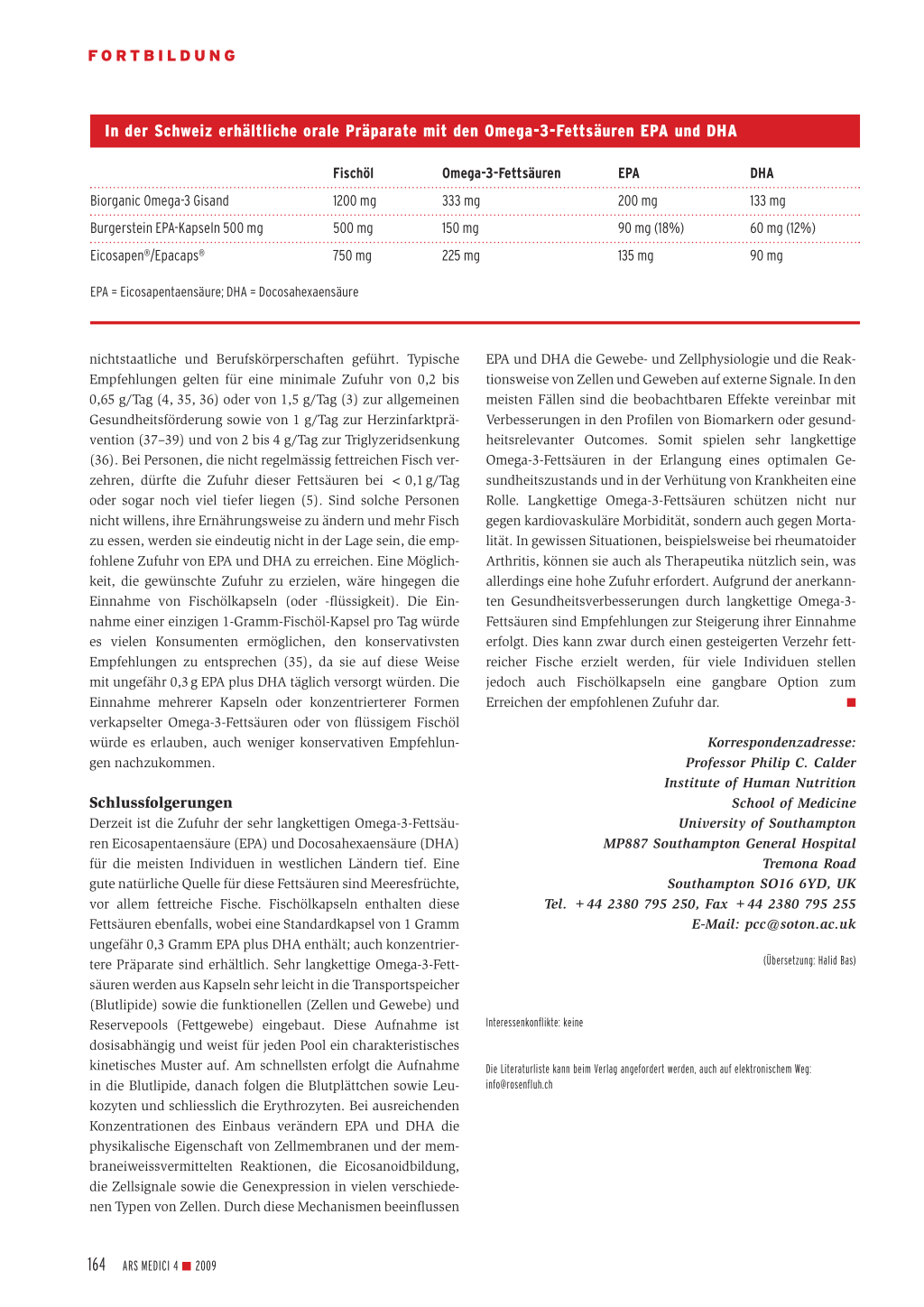
In der Schweiz erhältliche orale Präparate mit den Omega-3-Fettsäuren EPA und DHA
Biorganic Omega-3 Gisand Burgerstein EPA-Kapseln 500 mg Eicosapen®/Epacaps®
Fischöl 1200 mg 500 mg 750 mg
EPA = Eicosapentaensäure; DHA = Docosahexaensäure
Omega-3-Fettsäuren 333 mg 150 mg 225 mg
EPA 200 mg 90 mg (18%) 135 mg
DHA 133 mg 60 mg (12%) 90 mg
nichtstaatliche und Berufskörperschaften geführt. Typische Empfehlungen gelten für eine minimale Zufuhr von 0,2 bis 0,65 g/Tag (4, 35, 36) oder von 1,5 g/Tag (3) zur allgemeinen Gesundheitsförderung sowie von 1 g/Tag zur Herzinfarktprävention (37–39) und von 2 bis 4 g/Tag zur Triglyzeridsenkung (36). Bei Personen, die nicht regelmässig fettreichen Fisch verzehren, dürfte die Zufuhr dieser Fettsäuren bei < 0,1 g/Tag oder sogar noch viel tiefer liegen (5). Sind solche Personen nicht willens, ihre Ernährungsweise zu ändern und mehr Fisch zu essen, werden sie eindeutig nicht in der Lage sein, die empfohlene Zufuhr von EPA und DHA zu erreichen. Eine Möglichkeit, die gewünschte Zufuhr zu erzielen, wäre hingegen die Einnahme von Fischölkapseln (oder -flüssigkeit). Die Einnahme einer einzigen 1-Gramm-Fischöl-Kapsel pro Tag würde es vielen Konsumenten ermöglichen, den konservativsten Empfehlungen zu entsprechen (35), da sie auf diese Weise mit ungefähr 0,3 g EPA plus DHA täglich versorgt würden. Die Einnahme mehrerer Kapseln oder konzentrierterer Formen verkapselter Omega-3-Fettsäuren oder von flüssigem Fischöl würde es erlauben, auch weniger konservativen Empfehlungen nachzukommen. Schlussfolgerungen Derzeit ist die Zufuhr der sehr langkettigen Omega-3-Fettsäuren Eicosapentaensäure (EPA) und Docosahexaensäure (DHA) für die meisten Individuen in westlichen Ländern tief. Eine gute natürliche Quelle für diese Fettsäuren sind Meeresfrüchte, vor allem fettreiche Fische. Fischölkapseln enthalten diese Fettsäuren ebenfalls, wobei eine Standardkapsel von 1 Gramm ungefähr 0,3 Gramm EPA plus DHA enthält; auch konzentriertere Präparate sind erhältlich. Sehr langkettige Omega-3-Fettsäuren werden aus Kapseln sehr leicht in die Transportspeicher (Blutlipide) sowie die funktionellen (Zellen und Gewebe) und Reservepools (Fettgewebe) eingebaut. Diese Aufnahme ist dosisabhängig und weist für jeden Pool ein charakteristisches kinetisches Muster auf. Am schnellsten erfolgt die Aufnahme in die Blutlipide, danach folgen die Blutplättchen sowie Leukozyten und schliesslich die Erythrozyten. Bei ausreichenden Konzentrationen des Einbaus verändern EPA und DHA die physikalische Eigenschaft von Zellmembranen und der membraneiweissvermittelten Reaktionen, die Eicosanoidbildung, die Zellsignale sowie die Genexpression in vielen verschiedenen Typen von Zellen. Durch diese Mechanismen beeinflussen EPA und DHA die Gewebe- und Zellphysiologie und die Reak- tionsweise von Zellen und Geweben auf externe Signale. In den meisten Fällen sind die beobachtbaren Effekte vereinbar mit Verbesserungen in den Profilen von Biomarkern oder gesund- heitsrelevanter Outcomes. Somit spielen sehr langkettige Omega-3-Fettsäuren in der Erlangung eines optimalen Ge- sundheitszustands und in der Verhütung von Krankheiten eine Rolle. Langkettige Omega-3-Fettsäuren schützen nicht nur gegen kardiovaskuläre Morbidität, sondern auch gegen Morta- lität. In gewissen Situationen, beispielsweise bei rheumatoider Arthritis, können sie auch als Therapeutika nützlich sein, was allerdings eine hohe Zufuhr erfordert. Aufgrund der anerkann- ten Gesundheitsverbesserungen durch langkettige Omega-3- Fettsäuren sind Empfehlungen zur Steigerung ihrer Einnahme erfolgt. Dies kann zwar durch einen gesteigerten Verzehr fett- reicher Fische erzielt werden, für viele Individuen stellen jedoch auch Fischölkapseln eine gangbare Option zum Erreichen der empfohlenen Zufuhr dar. ■ Korrespondenzadresse: Professor Philip C. Calder Institute of Human Nutrition School of Medicine University of Southampton MP887 Southampton General Hospital Tremona Road Southampton SO16 6YD, UK Tel. +44 2380 795 250, Fax +44 2380 795 255 E-Mail: pcc@soton.ac.uk (Übersetzung: Halid Bas) Interessenkonflikte: keine Die Literaturliste kann beim Verlag angefordert werden, auch auf elektronischem Weg: info@rosenfluh.ch 164 ARS MEDICI 4 ■ 2009